EXPERT-C: A randomized phase II European multicenter trial of neoadjuvant chemotherapy (capecitabine/oxaliplatin) and chemoradiation (CRT) with or without cetuximab followed by total mesorectal excision (TME) in patients with MRI-defined high-risk rectal cancer.
Alice Dewdney, et al.
|
||||
直腸癌における短期間の術前放射線療法1)および化学放射線療法 (CRT) 2) は、いずれも局所再発率を低下させるが、OSへの影響については評価が定まっていない。我々は以前、MRIで予後不良と診断された直腸癌患者に対し、直腸間膜全切除 (total mesorectal excision: TME) および術前CRTの実施前後に化学療法を追加した治療を、シングルアームの第II相試験 (EXPERT試験) において検証し、忍容性があることを報告した3)。 |
||||
対象は、MRIによりハイリスクと診断された手術の可能な局所直腸癌 (腺癌) とし、下図の2群に無作為に割り付けた。 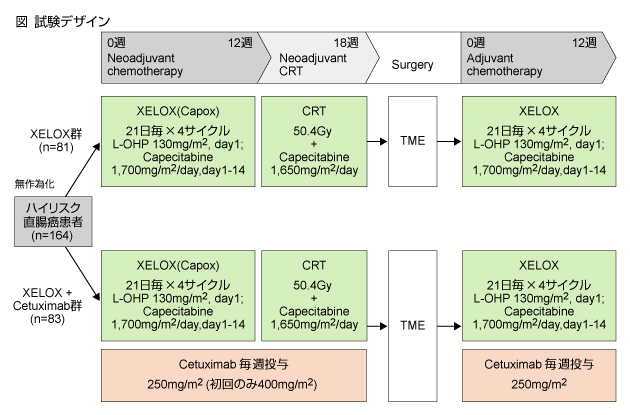
|
||||
|
2005年から2008年までに、欧州15施設から165例 (XELOX群81例、XELOX + Cetuximab群84例) が登録された。術前CRTを施行された患者はXELOX群で89%、Cetuximab併用群では94%であり、手術まで完遂できたのは各々89%、92%であった。 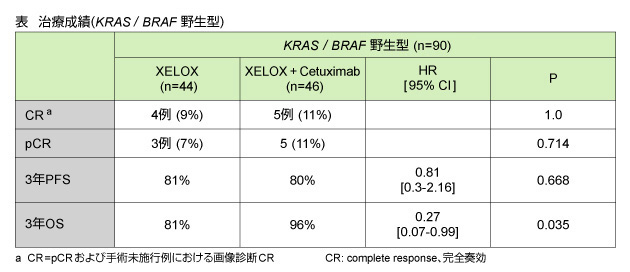
一次エンドポイントである野生型におけるCR率は、XELOX群で9%、Cetuximab併用群では11%であり (p=1.0)、またpCR率についても有意差は認められなかった (p=0.714)。 |
||||
一次エンドポイントである野生型におけるCR率およびpCR率については、両群間で有意差は認められなかったが、RRについては有意な改善が得られた。3年OSについても、Cetuximab併用群における有意な改善が認められた。 |
||||
Reference
1) Swedish Rectal Cancer Trial: N Engl J Med. 336(14): 980-987, 1997 [PubMed]
2) Bosset JF, et al.: N Engl J Med. 355(11): 1114-1123, 2006 [PubMed][論文紹介]
3) Chua YJ, et al.: Lancet Oncol. 11(3): 241-248, 2010 [PubMed]
4) Bonner JA, et al.: N Engl J Med. 354(6): 567-578, 2006 [PubMed]
5) Glynne-Jones, et al.: Acta Oncol. 49(3): 278-286, 2010 [PubMed]
【関連リンク】
ESMO 2010レポート
654P 「ハイリスク局所進行直腸癌患者に対する術前補助療法としての5-FU + Oxaliplatin + Panitumumab併用放射線療法を検討した第II相試験の最終報告 (STARPAN/STAR-02試験)」
論文紹介
直腸癌における術前放射線療法と化学療法の併用の有用性 (Bosset J-F, et al.: N Engl J Med. 2006)
論文紹介
切除不能直腸癌に対する術前放射線療法と術前化学放射線療法の無作為化第III相試験 (Brandengen M, et al.: J Clin Oncol. 2008)
論文紹介
MRIにより診断された局所進行直腸癌における同時化学放射線療法後の手術および術後補助CAPOX (capecitabine + oxaliplatin) と、導入CAPOX後に同時化学放射線療法および手術とを比較する第II相無作為化試験 (Fernández-Martos C, et al.: J Clin Oncol. 2010)
論文紹介
直腸癌への化学放射線療法施行後に病理学的完全奏効が得られた患者の長期予後: 個々の患者データのプール解析 (Maas M, et al.: Lancet Oncol. 2010)

