|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。
|

REGARD試験:プラチナ製剤またはフッ化ピリミジン系薬剤を含む併用療法後に進行した胃・胃食道接合部腺癌に対するBSC ± Ramucirumabの二重盲検プラセボ対照無作為化第III相試験
REGARD: A Phase III, Randomized, Double-Blind Trial of Ramucirumab and Best Supportive Care (BSC) versus Placebo and BSC in the Treatment of Metastatic Gastric or Gastroesophageal Junction (GEJ) Adenocarcinoma Following Disease Progression on First-Line Platinum- or Fluoropyrimidine-Containing Combination Therapy.
Charles S Fuchs, et al.

抗VEGFR-2抗体薬が胃癌患者の生存を延長

本邦の胃癌化学療法では、1st-lineはS-1 + CDDP療法が標準で、2nd-line、3rd-lineにCPT-11、タキサン系薬剤を用いることが一般的である。そのためBSC対象の結果だけでは本邦に受け入れがたい点が指摘されている。現在、胃癌2nd-lineにおけるPaclitaxel ± Ramucirumabの第III相試験 (RAINBOW試験) が本邦を含めた国際共同治験として行われており、その結果に期待される。
胃癌は癌死の主要因の1つであり1)、患者の2/3が診断時に進行または転移を有することが知られている。血管内皮細胞増殖因子 (VEGF) を介するシグナル伝達および血管新生は胃癌の発症機序に関与している可能性がある2)。また、VEGF受容体 (VEGFR-2) とそのリガンド (VEGF-A、VEGF-C、VEGF-Dなど) は血管新生の主なメディエータであり、胃癌における重要な治療標的となる可能性がある3)。
RamucirumabはVEGFR-2の細胞外ドメインに結合する完全ヒト化IgG1モノクローナル抗体であり、VEGFリガンドの結合を遮断し、受容体の活性化を阻害する4, 5)。治療抵抗性の進行固形癌を対象とした2つの第I相試験において、Ramucirumabは良好な忍容性を示すとともに、40%の症例で5ヵ月以上の病勢コントロールを達成している6)。
REGARD試験は、プラチナ製剤またはフッ化ピリミジン系薬剤を含む併用療法後に進行した胃・胃食道接合部腺癌に対する2nd-line治療におけるRamucirumabの安全性と有効性を評価する、国際的な多施設共同二重盲検プラセボ対照無作為化第III相試験である。
RamucirumabはVEGFR-2の細胞外ドメインに結合する完全ヒト化IgG1モノクローナル抗体であり、VEGFリガンドの結合を遮断し、受容体の活性化を阻害する4, 5)。治療抵抗性の進行固形癌を対象とした2つの第I相試験において、Ramucirumabは良好な忍容性を示すとともに、40%の症例で5ヵ月以上の病勢コントロールを達成している6)。
REGARD試験は、プラチナ製剤またはフッ化ピリミジン系薬剤を含む併用療法後に進行した胃・胃食道接合部腺癌に対する2nd-line治療におけるRamucirumabの安全性と有効性を評価する、国際的な多施設共同二重盲検プラセボ対照無作為化第III相試験である。
対象は、1st-line治療終了後4ヵ月以内または術後補助化学療法終了後6ヵ月以内にPDとなった胃・胃食道接合部腺癌患者であり、Ramucirumab (8mg/kg静注投与、2週毎) + BSCを施行 (Ramucirumab群) 、またはplacebo (2週毎) + BSCを施行 (placebo群) とに、2:1の割合で無作為に割り付けられた (図1) 。主要評価項目はOS、副次評価項目はPFS、12週PFS、奏効率、安全性などであった。
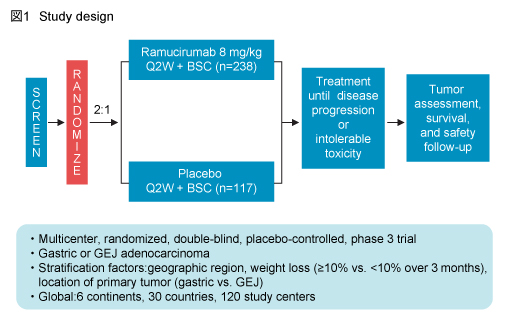
2009年10月から2012年1月までに355例が登録され、Ramucirumab群に238例、placebo群に117例が割り付けられた。ベースライン時の患者背景はバランスがとれていた。
主要評価項目であるOS中央値はRamucirumab群5.2ヵ月、placebo群3.8ヵ月であり、Ramucirumab群で有意な延長を認めた (HR=0.776, 95% CI: 0.603-0.998, p=0.0473) (図2) 。
主要評価項目であるOS中央値はRamucirumab群5.2ヵ月、placebo群3.8ヵ月であり、Ramucirumab群で有意な延長を認めた (HR=0.776, 95% CI: 0.603-0.998, p=0.0473) (図2) 。
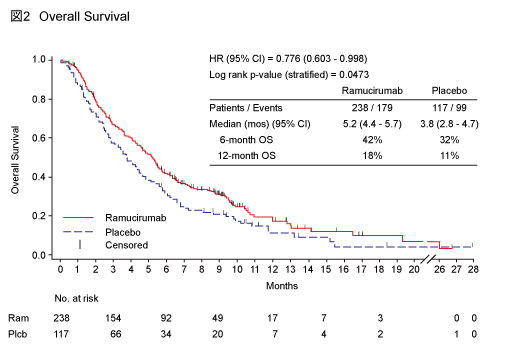
副次評価項目のPFSもRamucirumab群2.1ヵ月、placebo群1.3ヵ月と、Ramucirumab群で有意な延長を認めた (HR=0.483, 95% CI: 0.376-0.620, p<0.0001) (図3) 。また、12週PFSはRamucirumab群40%、placebo群16%だった。
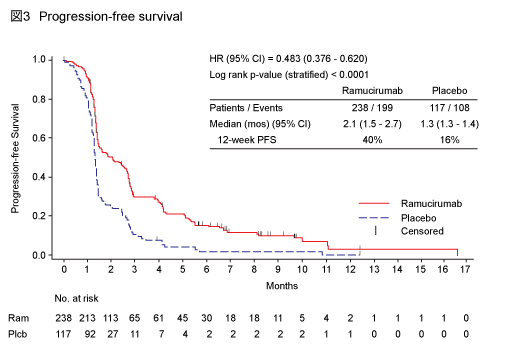
奏効率はRamucirumab群3.4%、placebo群2.6%と、両群で差は認められなかったが (p=0.756) 、病勢コントロール率はRamucirumab群48.7%、placebo群23.1%と、Ramucirumab群で有意に良好であった (p<0.0001) 。なお、後治療を受けた割合は、Ramucirumab群は31.5%であり、placebo群の39.3%に比べ低い傾向にあった。
有害事象による死亡はRamucirumab群10.6%、placebo群13.0%であった。死因となった有害事象は、Ramucirumab群では菌血症、心停止、胆管炎、胆汁うっ滞、脱水、呼吸困難、消化管の出血・閉塞・穿孔、負傷、心筋梗塞、多臓器不全、肺炎、腎不全が認められ、placebo群では呼吸困難、消化管の出血・閉塞・穿孔、多臓器不全、肺塞栓症、肺炎、呼吸器不全、敗血性ショック、突然死が確認された。
治療関連有害事象の頻度は両群でほぼ同等であった。また、血管新生阻害薬や抗体医薬で一般的にみられる有害事象の発現状況についても、両群で類似していた (表) 。なお、grade 3以上の高血圧はRamucirumab群で高い傾向にあったが、grade 3が7.6%であり、grade 4はみられなかった。
有害事象による死亡はRamucirumab群10.6%、placebo群13.0%であった。死因となった有害事象は、Ramucirumab群では菌血症、心停止、胆管炎、胆汁うっ滞、脱水、呼吸困難、消化管の出血・閉塞・穿孔、負傷、心筋梗塞、多臓器不全、肺炎、腎不全が認められ、placebo群では呼吸困難、消化管の出血・閉塞・穿孔、多臓器不全、肺塞栓症、肺炎、呼吸器不全、敗血性ショック、突然死が確認された。
治療関連有害事象の頻度は両群でほぼ同等であった。また、血管新生阻害薬や抗体医薬で一般的にみられる有害事象の発現状況についても、両群で類似していた (表) 。なお、grade 3以上の高血圧はRamucirumab群で高い傾向にあったが、grade 3が7.6%であり、grade 4はみられなかった。
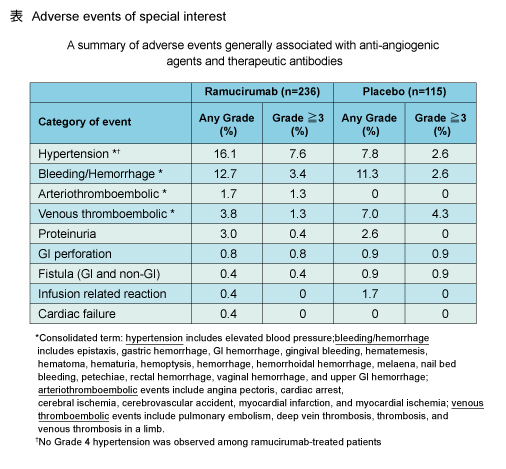
Ramucirumabは、プラチナ製剤またはフッ化ピリミジン系薬剤を含む併用療法後に進行した胃・胃食道接合部腺癌の2nd-line治療において、placeboに対してOS (HR=0.776, p=0.0473) およびPFS (HR=0.483, p<0.0001) で統計学的に有意なbenefitをもたらした。また、安全性に関しては、予期せぬ新たな知見はみられなかった。
以上より、Ramucirumabは胃・胃食道接合部腺癌の新たな2nd-line治療となる可能性あると考えられる。
以上より、Ramucirumabは胃・胃食道接合部腺癌の新たな2nd-line治療となる可能性あると考えられる。
Reference
1) American Cancer Society 2012
2) Jüttner S, et al.: J Clin Oncol. 24(2): 228-240, 2006 [PubMed]
3) Youssoufian H, et al.: Clin Cancer Res. 13(suppl 18): 5544s-5548s, 2007 [PubMed]
4) Lu D, et al.: J Biol Chem. 278(44): 43496-43507, 2003 [PubMed]
5) Zhu Z, et al.: Leukemia. 17(3): 604-611, 2003 [PubMed]
6) Spratlin JL, et al.: J Clin Oncol. 28(5): 780-787, 2010 [PubMed]
1) American Cancer Society 2012
2) Jüttner S, et al.: J Clin Oncol. 24(2): 228-240, 2006 [PubMed]
3) Youssoufian H, et al.: Clin Cancer Res. 13(suppl 18): 5544s-5548s, 2007 [PubMed]
4) Lu D, et al.: J Biol Chem. 278(44): 43496-43507, 2003 [PubMed]
5) Zhu Z, et al.: Leukemia. 17(3): 604-611, 2003 [PubMed]
6) Spratlin JL, et al.: J Clin Oncol. 28(5): 780-787, 2010 [PubMed]
