
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
EGFRシグナル伝達経路の変異:FIRE-3試験における有効性への影響 -KRAS exon 2野生型の切除不能進行・再発大腸癌に対する1st-lineとしてのFOLFIRI + CetuximabおよびFOLFIRI + Bevacizumabの無作為化第III相試験
Mutations within the EGFR Signaling Pathway: Influence on Efficacy in FIRE-3 - A Randomized Phase III Study of FOLFIRI Plus Cetuximab or Bevacizumab as First-line Treatment for Wild-type (WT) KRAS (exon 2) Metastatic Colorectal Cancer (mCRC) Patients
Sebastian Stintzing, et al.

新たなバイオマーカー探索の重要性

RAS のminor変異に注目することが推奨されるなか、EGFR伝達経路のその他のバイオマーカー探索が求められている。BRAF やPIK3CA はその候補として注目されているが、もともとの数が少ないため、結論を導き出すことは難しい。今回の発表も、ESMOでの知見にこの点が加わったことが新しいだけではある。しかしながら、新薬開発を進めていくうえで、このような解析を行っていくこと、可能な限り全ての症例のバイオマーカー探索ができるような臨床試験のあり方は、今後ますます重要になっていくと思われる。
FIRE-3試験は、KRAS exon 2野生型の切除不能進行・再発大腸癌に対する1st-lineにおいてFOLFIRI + Cetuximab (Cetuximab群) とFOLFIRI + Bevacizumab (Bevacizumab群) を比較した第III相試験である (図1)。主要評価項目である奏効率、副次評価項目であるPFSでは両群間に差を認めなかったものの、OSはCetuximab群で有意な延長を認めた (HR=0.77, p=0.017) (過去レポート)。
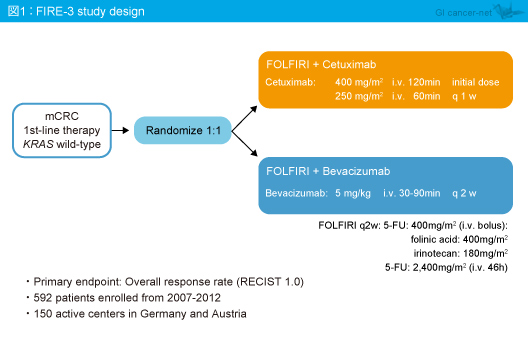
FIRE-3試験では、EGFRシグナル伝達経路の遺伝子変異の有無による有効性解析の実施が事前に設定されている。今回、ESMO2013で報告されたKRAS (exon 2, 3, 4)、NRAS (exon 2, 3, 4)、BRAF (V600E) の変異の有無とともに、PIK3CA (exon 9, 20)、AKT (E17K) の変異についても評価し、その上でFIRE-3試験の奏効率、PFS、OSが検証された。
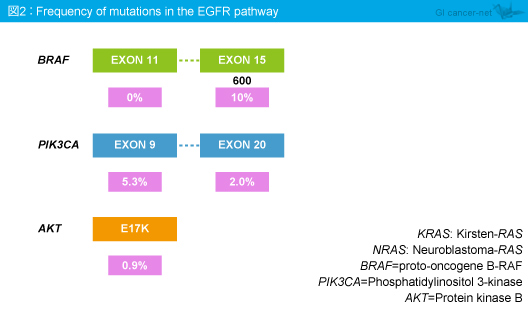
ITT解析対象 (KRAS exon 2野生型) は592例であり、本検討では407例 (69%) について遺伝子解析評価が実施された。遺伝子変異は、BRAF exon 11: 0%, exon 15: 10%、PIK3CA exon 9: 5.3%, exon 20: 2.0%、AKT E17K: 0.9%に認められ (図2)、図3のように分布していた。
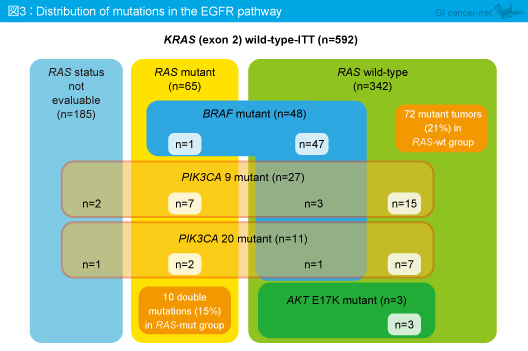
KRAS (exon 2, 3, 4)、NRAS (exon 2, 3, 4) の解析においては、FIRE-3試験の主要評価項目である奏効率は、RAS 野生型ではCetuximab群が、RAS 変異型ではBevacizumab群で奏効率が高いことが示された (過去レポート)。また、RAS 野生型においてCetuximab群はBevacizumab群に比してOSの有意な延長が認められ、その差は7.5ヵ月であった (HR=0.70, 95% CI: 0.53-0.92, p=0.011) (過去レポート)。
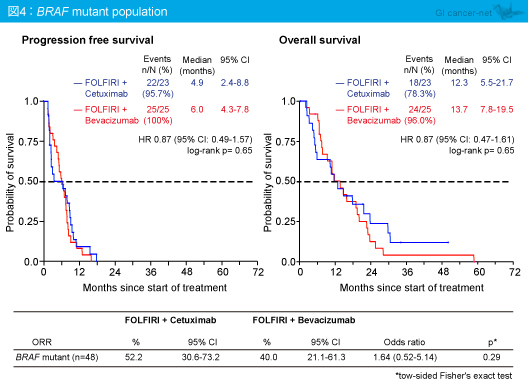
BRAF 変異型では、奏効率はCetuximab群52.2%、Bevacizumab群40.0% (OR=1.64, 95% CI: 0.52-5.14, p=0.29)、PFS中央値はそれぞれ4.9ヵ月、6.0ヵ月 (HR=0.87, 95% CI: 0.49-1.57, p=0.65)、OS中央値は12.3ヵ月、13.7ヵ月であり (HR=0.87, 95% CI: 0.47-1.61, p=0.65)、いずれも差が認められなかった (図4)。
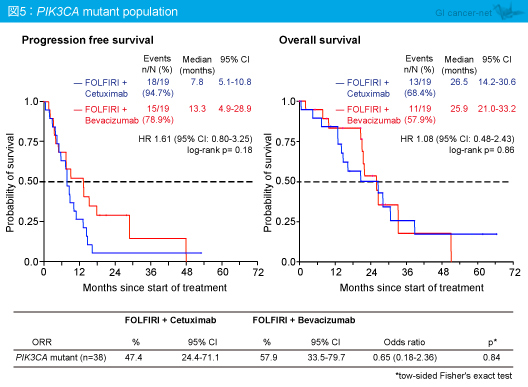
PIK3CA 変異型では、奏効率はCetuximab群47.4%、Bevacizumab群57.9% (OR=0.65, 95% CI: 0.18-2.36, p=0.84) であり、OS中央値はそれぞれ26.5ヵ月、25.9ヵ月と、両群間に差を認めなかった (HR=1.08, 95% CI: 0.48-2.43, p=0.86)。また、PFS中央値はそれぞれ7.8ヵ月、13.3ヵ月 (HR=1.61, 95% CI: 0.80-3.25, p=0.18) であり、Bevacizumab群で優れる傾向にあったものの有意差は認められなかった (図5)。
RAS (KRAS 、NRAS ) 遺伝子の事前検査は、切除不能進行・再発大腸癌患者への治療に際して高く推奨され、RAS 野生型患者の1st-lineにおけるFOLFIRI + Cetuximab療法は生存期間の延長に寄与する。BRAF 、PIK3CA 変異型患者は少数であるため、明確な結論は得られないものの、CetuximabとBevacizumabでは同程度のOSが得られることが示された。
