
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
Bevacizumabベースの治療を受けた切除不能進行・再発大腸癌患者における初回増悪後のBevacizumab + 化学療法継続:ML18147試験におけるKRAS statusおよび1st-line化学療法による治療効果
Bevacizumab + Chemotherapy Continued beyond First Disease Progression in Patients with Metastatic Colorectal Cancer Previously Treated with Bevacizumab-based Therapy: Outcomes According to KRAS Status and Chemotherapy Backbone in the ML18147 Study
Stefan Kubicka, et al.
Bevacizumabの2nd-line継続使用へ尽きぬ臨床的興味

KRAS statusにかかわらず継続使用が有効であるのならば、なおさら2nd-lineにおける抗VEGF抗体薬のバイオマーカーの存在についても検討課題である。WJOGで行われている、BevacizumabとPanitumumabの2nd-lineにおける比較試験1)が、その疑問に少しでも鍵を見出してくれることを期待している。
切除不能進行・再発大腸癌に対する1st-lineおよび2nd-lineでは、標準的な化学療法レジメンにBevacizumabを併用することで、治療効果を改善することが示されている1-3)。
ML18147 (TML) 試験は、1st-lineでBevacizumabを含む化学療法後増悪した患者に対して、2nd-lineもBevacizumabを含む化学療法を継続投与することで、OSが有意に延長することを示した初めての第III相試験である4)。
ML18147試験では、化学療法におけるOxaliplatin (L-OHP) またはIrinotecan (CPT-11) ベースの治療選択は主治医判断であり、2nd-lineではこれらをクロスオーバーして投与することとしている。2nd-lineの治療法として確立されたフッ化ピリミジン系製剤 + L-OHP/CPT-11ベースのレジメンは、いずれも以下の認識のもとで使用されている。
ML18147試験では探索的バイオマーカー研究が含まれており、腫瘍組織、血漿、血液検査が実施されている。この背景として、抗EGFR抗体薬はKRAS 野生型に有益であるものの、KRAS 変異型では有益ではないこと7-9)、KRAS 変異型は2nd-lineでの予後因子となり得るか解明されていないこと10)、従来の報告ではBevacizumabの有効性はKRAS 変異に依存しないとされていることなどが挙げられる11-13)。
そこで、今回の探索的研究では、KRAS 変異の有無および併用化学療法が及ぼす影響を検証することを目的とした。
ML18147 (TML) 試験は、1st-lineでBevacizumabを含む化学療法後増悪した患者に対して、2nd-lineもBevacizumabを含む化学療法を継続投与することで、OSが有意に延長することを示した初めての第III相試験である4)。
ML18147試験では、化学療法におけるOxaliplatin (L-OHP) またはIrinotecan (CPT-11) ベースの治療選択は主治医判断であり、2nd-lineではこれらをクロスオーバーして投与することとしている。2nd-lineの治療法として確立されたフッ化ピリミジン系製剤 + L-OHP/CPT-11ベースのレジメンは、いずれも以下の認識のもとで使用されている。
| ・ | CPT-11、L-OHPともに切除不能進行・再発大腸癌の1st-lineにおける有効性は同等であるが5)、有害事象プロファイルは異なっており、一般的にL-OHPでは蓄積性の神経毒性が、CPT-11では消化器症状がみられる。 |
| ・ | 使用する化学療法は、治療歴と患者の嗜好性によって選択されることが一般的である6)。 |
そこで、今回の探索的研究では、KRAS 変異の有無および併用化学療法が及ぼす影響を検証することを目的とした。
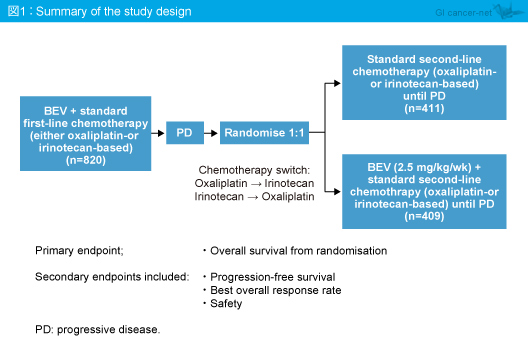
ML18147試験は、欧州とサウジアラビアの220施設が参加した第III相試験である。切除不能進行・再発大腸癌症例に対して1st-lineでBevacizumabを含む化学療法が実施され、投与中止から3ヵ月以内の症例を対象に、Bevacizumab併用群と化学療法単独群に割り付けられた (図1)。
今回のpost-hoc解析では、併用化学療法 (L-OHP/CPT-11ベース) およびKRAS 変異によるOS、PFS、奏効率、病勢コントロール率の検討を目的とし、KRAS 変異については、Scorpion ARMS法によりKRAS exon 2 (codon12, 13) を評価している。なお、KRAS statusによるサブグループの探索的解析は、治療効果の一貫性をみることを企図したため、ML18147試験の主要評価項目および副次評価項目が検討され、多重検定の調整は行わず、統計的有意差の検出力は持たなかった。
今回のpost-hoc解析では、併用化学療法 (L-OHP/CPT-11ベース) およびKRAS 変異によるOS、PFS、奏効率、病勢コントロール率の検討を目的とし、KRAS 変異については、Scorpion ARMS法によりKRAS exon 2 (codon12, 13) を評価している。なお、KRAS statusによるサブグループの探索的解析は、治療効果の一貫性をみることを企図したため、ML18147試験の主要評価項目および副次評価項目が検討され、多重検定の調整は行わず、統計的有意差の検出力は持たなかった。
2006年2月〜2010年6月の間にML18147試験に登録された820例中616例 (ITT解析の75%) が対象となった。KRAS statusは、KRAS 野生型316例、KRAS 変異型300例であり、2nd-lineの化学療法は、L-OHPが355例、CPT-11が261例であった。
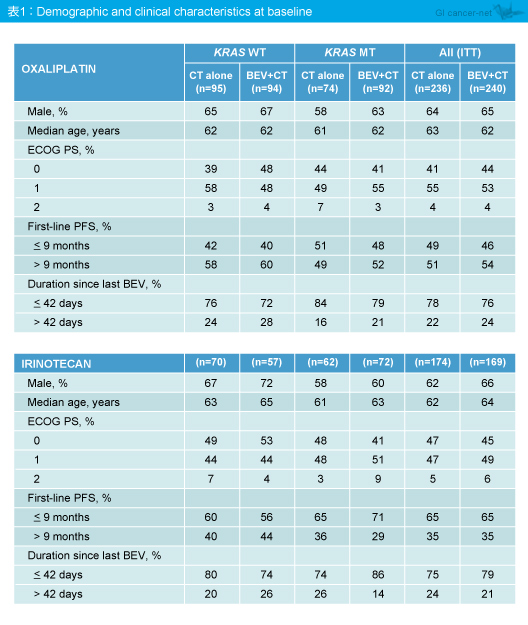
KRAS status別、化学療法別における患者背景は表1の通りである。1st-lineにおけるPFSが9ヵ月以内の症例は、L-OHP治療例に比べてCPT-11治療例で多かった。
KRAS status別、化学療法別における患者背景は表1の通りである。1st-lineにおけるPFSが9ヵ月以内の症例は、L-OHP治療例に比べてCPT-11治療例で多かった。
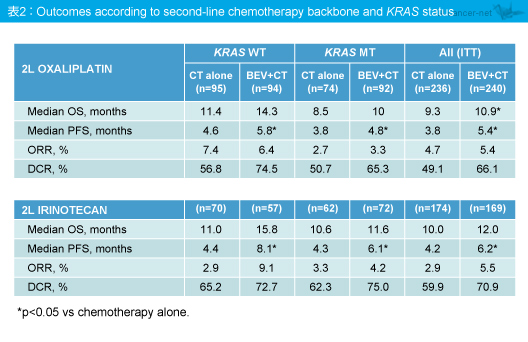
KRAS status、併用した化学療法にかかわらず、Bevacizumab併用群は化学療法単独群に比べて、OS、PFSともに良好であった (表2)。
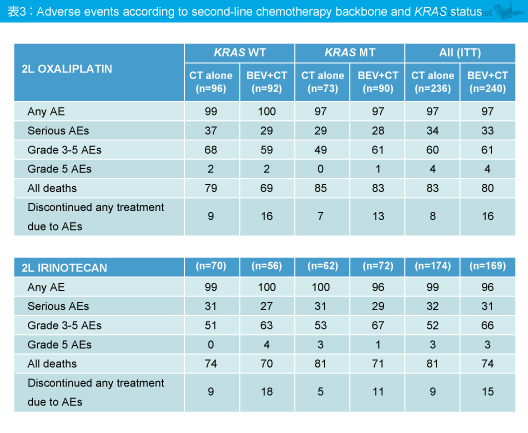
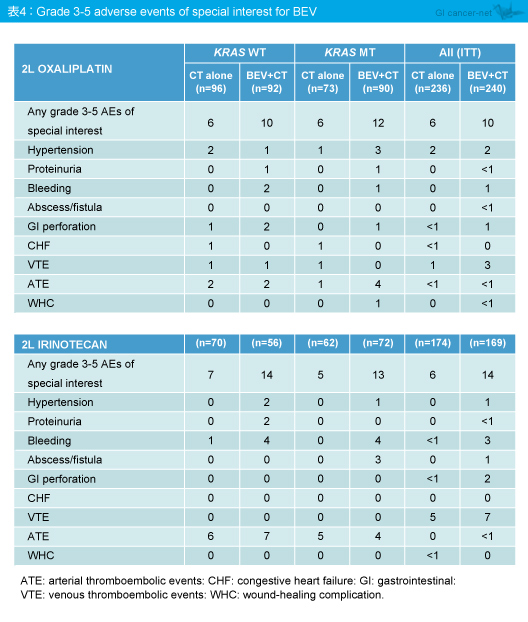
一般的な有害事象およびBevacizumab特有の有害事象について、Bevacizumab継続使用による増加はみられなかった (表3、4)。
今回のpost-hoc解析により、2nd-lineにおけるBevacizumabの継続使用は、KRAS status、2nd-lineで使用する化学療法によらずOSとPFSを延長すること、Bevacizumab継続使用による新たな有害事象の発現ならびに発現頻度の違いは生じないことが示された。
Reference
1) Hurwitz H, et al.: N Engl J Med. 350(23): 2335-2342, 2004[PubMed]
2) Saltz LB, et al.: J Clin Oncol. 26(12): 2013-2019, 2008[PubMed]
3) Giantonio BJ, et al.: J Clin Oncol. 25(12): 1539-1544, 2007[PubMed]
4) Bennouna J, et al.: Lancet Oncol. 14(1): 29-37, 2013[PubMed]
5) Tournigand C, et al.: J Clin Oncol. 22(2): 229-237, 2004[PubMed]
6) Punt CJ.: Ann Oncol. 16(6): 845-846, 2005[PubMed]
7) Karapetis CS, et al.: N Engl J Med. 359(17): 1757-1765, 2008[PubMed]
8) Van Cutsem E, et al.: J Clin Oncol. 29(15): 2011-2019, 2011[PubMed]
9) Douillard JY, et al.: J Clin Oncol. 28(31): 4697-4705, 2010[PubMed]
10) Amado RG, et al.: J Clin Oncol. 26(10): 1626-1634, 2008[PubMed]
11) Hurwitz HI, et al.: Oncologist. 14(1): 22-28, 2009[PubMed]
12) Price TJ, et al.: J Clin Oncol. 29(19): 2675-2682, 2011[PubMed]
13) Kubicka S, et al.: Ann Oncol. 24(9): 2342-2349, 2013[PubMed]
1) Hurwitz H, et al.: N Engl J Med. 350(23): 2335-2342, 2004[PubMed]
2) Saltz LB, et al.: J Clin Oncol. 26(12): 2013-2019, 2008[PubMed]
3) Giantonio BJ, et al.: J Clin Oncol. 25(12): 1539-1544, 2007[PubMed]
4) Bennouna J, et al.: Lancet Oncol. 14(1): 29-37, 2013[PubMed]
5) Tournigand C, et al.: J Clin Oncol. 22(2): 229-237, 2004[PubMed]
6) Punt CJ.: Ann Oncol. 16(6): 845-846, 2005[PubMed]
7) Karapetis CS, et al.: N Engl J Med. 359(17): 1757-1765, 2008[PubMed]
8) Van Cutsem E, et al.: J Clin Oncol. 29(15): 2011-2019, 2011[PubMed]
9) Douillard JY, et al.: J Clin Oncol. 28(31): 4697-4705, 2010[PubMed]
10) Amado RG, et al.: J Clin Oncol. 26(10): 1626-1634, 2008[PubMed]
11) Hurwitz HI, et al.: Oncologist. 14(1): 22-28, 2009[PubMed]
12) Price TJ, et al.: J Clin Oncol. 29(19): 2675-2682, 2011[PubMed]
13) Kubicka S, et al.: Ann Oncol. 24(9): 2342-2349, 2013[PubMed]
