
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
KRAS 野生型の切除不能進行・再発大腸癌に対する3rd-lineにおけるPanitumumabの皮膚障害に関する無作為化比較試験:HGCSG1001試験 (J-STEPP試験)
Randomized Controlled Trial on the Skin Toxicity of Panitumumab in Third-line Treatment of KRAS Wild-type Metastatic Colorectal Cancer: HGCSG1001 (Japanese Skin Toxicity Evaluation Protocol with Panitumumab: J-STEPP)
Ichiro Iwanaga, et al.
(写真は共同演者のYoshito Komatsu氏)
(写真は共同演者のYoshito Komatsu氏)

STEPP試験の結果を本邦でも再現!

本会で発表されたJ-STEPP試験は、まさにその疑問に答える報告であった。本試験は日本人を対象に行われ、KRAS exon 2野生型で3rd-lineにPanitumumabを使用する症例を対象に、STEPP試験同様、皮膚障害 発現後に治療介入する対症療法群と、予防療法群における皮膚障害発現状況が比較検討された。6週時点におけるgrade 2以上の皮膚障害は、対症療法群の62.5%に対し、予防的療法群で21.3%とSTEPP試験同様、有意な差をもって予防効果を示した (risk ratio=0.34, p<0.001)。また、本試験において特筆すべきは、全ての情報を盲検化した上での皮膚科専門医による独立した評価であり、その評価も研究者評価と同様の結果 (対症療法群50.0% vs. 予防的療法群18.6%; risk ratio=0.37, p=0.002) を示していることである。オープンラベルの試験では研究者の意図的な判断が働くこともあるが、本試験ではこの解析によってデータの信頼性を強くしているものと思われた。
残念ながら、今回の発表において抗腫瘍効果の報告はなかったが、抗腫瘍効果に両群間で差がなければ、日本人においても予防的皮膚ケアを行うことが、QOL/治療継続性に与える影響を減じ、抗EGFR抗体薬の有効性を最大限発揮できることにつながるものと思われる。
PanitumumabはKRAS 野生型の切除不能進行・再発大腸癌に対して効果を発揮することが示されており1)、STEPP試験では皮膚障害に対する予防療法は対症療法と比較し、皮膚障害の発現を抑制することが示されている2)。一方、アジア人を対象とした予防療法に関するデータは存在しないため、本試験では日本人の切除不能・進行再発大腸癌患者を対象として、Panitumumabを含む化学療法施行時における皮膚障害の発現を、予防療法と対症療法で比較検討した。
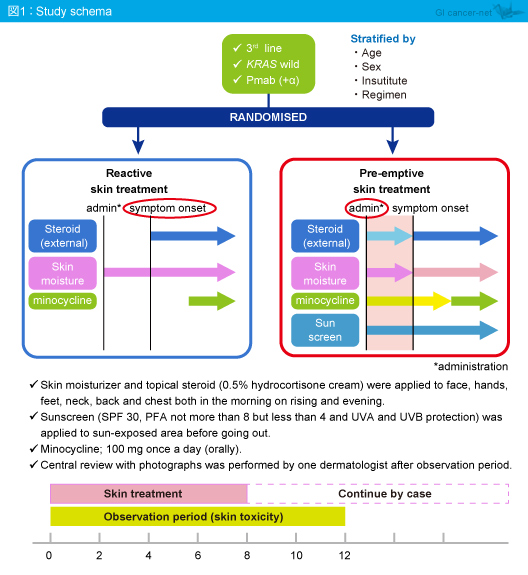
対象は、20歳以上、ECOG PS 0-2で日本人のKRAS 野生型切除不能進行・再発大腸癌患者で、3rd-lineにおいてPanitumumabを含む治療が実施された症例とした。年齢、性別、施設、レジメンで層別化して、皮膚障害の対症療法群と予防療法群に無作為に割り付けられた (図1)。
なお、各群における皮膚障害に対する治療は以下のとおりで、観察期間終了後に1人の皮膚科専門医が写真による中央判定を行った。
主要評価項目は、試験開始6週間におけるgrade 2以上の皮膚障害発現率であり、副次評価項目はgrade毎の皮膚障害初発までの期間、中央判定における皮膚障害であった。
STEPP試験の試験開始6週間におけるgrade 2以上の皮膚障害発現率は、対症療法群62%、予防療法群29%であったため、皮膚障害発現率の期待値を29%、閾値を62%とし、検出力90%、両側5%の有意水準で必要登録例は92例となり、不適格症例を10%考慮して目標症例数は102例とした。
なお、各群における皮膚障害に対する治療は以下のとおりで、観察期間終了後に1人の皮膚科専門医が写真による中央判定を行った。
| ・ | 対症療法群 |
| Panitumumab投与開始時より保湿剤を塗布し、皮膚障害発現後にステロイドを塗布し、ミノサイクリンを内服する。 | |
| ・ | 予防療法群 |
| Panitumumab投与開始時より、保湿剤およびステロイド (ヒドロコルチゾン0.5%) を1日2回、顔、手足、首、背、胸に塗布し、日焼け止め (SPF: 30、PFA: 4〜8) を外出時に塗布。そしてミノサイクリン (100mg/日) を内服する。 |
STEPP試験の試験開始6週間におけるgrade 2以上の皮膚障害発現率は、対症療法群62%、予防療法群29%であったため、皮膚障害発現率の期待値を29%、閾値を62%とし、検出力90%、両側5%の有意水準で必要登録例は92例となり、不適格症例を10%考慮して目標症例数は102例とした。
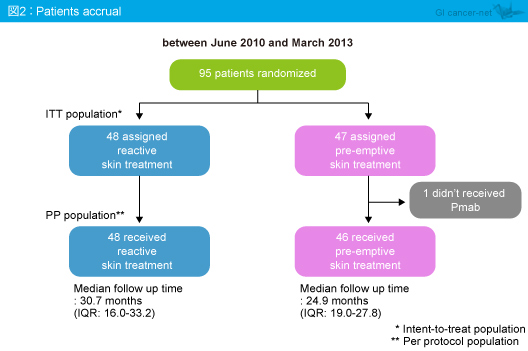
2010年6月〜2013年3月までに95例が登録され、対症療法群48例、予防療法群47例に割り付けられた。なお、予防療法群のうち1例はPanitumumabが投与されなかったため、46例が解析対象となった (図2)。
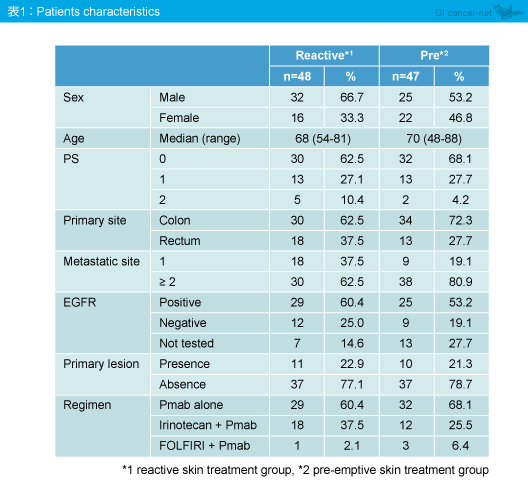
患者背景は両群間に差はみられなかった (表1)。
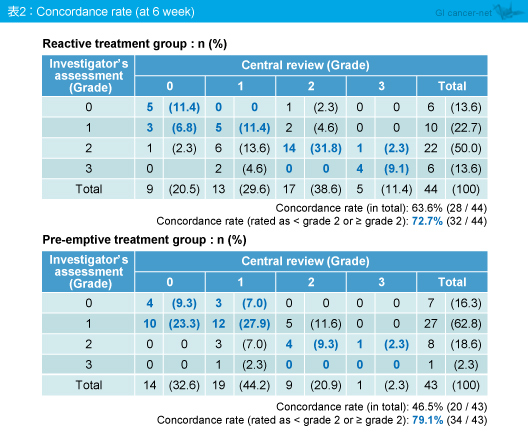
Panitumumab投与後6週間における皮膚障害の発現は、主治医判定と中央判定の双方で検討したが、両判定におけるgrade 2未満とgrade 2以上の皮膚障害発現の一致率は、対症療法群72.7%、予防療法群79.1%であった (表2)。
試験開始6週間におけるgrade 2以上の皮膚障害の発現率は、主治医判定で対症療法群62.5%、予防療法群21.3% (risk ratio=0.34, 95% CI: 0.19-0.62, p<0.001)、中央判定で対症療法群50.0%、予防療法群18.6% (risk ratio=0.37, 95% CI: 0.19-0.74, p=0.002) であり、いずれも予防療法群は対症療法群と比較し有意に低率であった (表3)。

