
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
S-1を含む1st-line治療に抵抗性となった進行・再発胃癌に対する2nd-lineとしてのCPT-11単独 vs. CPT-11 + S-1の第III相試験 (JACCRO GC-05試験)
A Randomized Phase III Trial of Second-line Chemotherapy Comparing CPT-11 Alone versus S-1 plus CPT-11 Combination Therapy in Advanced Gastric Cancer Refractory to First-line Therapy with S-1 (JACCRO GC-05)
Kazuhiro Nishikawa, et al.

2nd-line以降へのS-1継続使用に待った

結果、CPT-11 + S-1群はCPT-11群と比較して主要評価項目のOSだけでなく奏効率、PFSもほぼ同等であった。一方、grade 3以上の白血球減少、発熱性好中球減少症の頻度はCPT-11 + S-1群で有意に高かった。本試験のCPT-11 + S-1療法はCPT-11 (150mg/m2) を3週毎の投与法であり、CPT-11群 (同用量を2週毎) と比較してCPT-11の投与量は2/3となる。Key drugであるCPT-11の投与量が少なかったことが効果の上乗せがなかった要因かもしれないが、毒性を勘案するとS-1と併用する場合に本試験の設定以上にCPT-11投与量を増やすことは困難だろう。
胃癌のkey drugであるS-1を2nd-line以降も継続使用する治療は、確固たるエビデンスがないにもかかわらず、現在も実地臨床で行われているケースがある。本結果より、S-1の2nd-line以降への継続使用の有用性ははっきりと否定されたと考える。この点で、本試験はnegativeな結果に終わったが、本邦の実地臨床に大きく貢献する意義深い臨床試験であった。
東アジアでは、SPIRITS試験2)の結果に基づき、進行・再発胃癌に対する化学療法の1st-lineとしてS-1 + CDDPが標準的に用いられている。また、S-1を用いた1st-line後に増悪した場合には、2nd-lineでタキサン系製剤またはCPT-11の単独療法を用いることが多い。
一方、レトロスペクティブ解析ではあるが、1st-lineでS-1を含む化学療法を実施した後に増悪した症例に対して、2nd-lineでS-1を含む化学療法を行うことでOSが延長したとの報告があり3)、また、第I相試験の段階ではあるが、1st-lineにおけるCPT-11 + S-1の有効性が示されたとする報告もある4)。
一方、レトロスペクティブ解析ではあるが、1st-lineでS-1を含む化学療法を実施した後に増悪した症例に対して、2nd-lineでS-1を含む化学療法を行うことでOSが延長したとの報告があり3)、また、第I相試験の段階ではあるが、1st-lineにおけるCPT-11 + S-1の有効性が示されたとする報告もある4)。
対象は、20歳以上、ECOG PS ≦1で、1st-line としてのS-1を含む化学療法 (CPT-11 + S-1を除く) に治療抵抗性を示した切除不能進行・再発胃癌患者であり、S-1の用量は単剤として2,240mg/m2 (80mg/m2を4週相当) 以上、または併用療法として1,680mg/m2 (80mg/m2を3週相当) 以上の症例とした。なお、術後補助化学療法としてS-1を含む化学療法を行った症例は除外された。
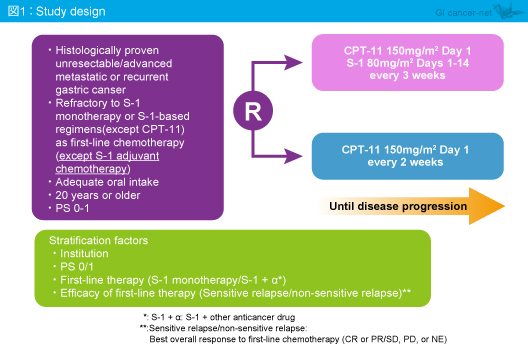
2nd-lineとしてCPT-11 (150mg/m2, day 1) およびS-1 (80mg/m2, day 1-14) を3週毎に投与する群 (CPT-11 + S-1群) と、CPT-11 (150mg/m2, day 1) を2週毎に投与する群 (CPT-11群) に、無作為に割り付けられ、増悪するまで投与された (図1)。
本試験は第II相/第III相試験として実施されており、主要評価項目は、第II相試験が6週時点におけるPD例の割合、第III相試験がOSであった。また、副次評価項目は、PFS、TTF (time to treatment failure: 治療成功期間)、奏効率、安全性、3rd-lineへの移行割合であった。
第II相部分は、PD例の割合の閾値60%として、目標症例数は60例であった。第III相試験は、CPT-11 + S-1群、CPT-11群におけるOS中央値をそれぞれ7ヵ月、5ヵ月と想定し、登録期間2年、追跡期間2年、両側α=0.05、検出力80%として、目標症例数は300例 (第II相試験の症例を含む) であった。
2nd-lineとしてCPT-11 (150mg/m2, day 1) およびS-1 (80mg/m2, day 1-14) を3週毎に投与する群 (CPT-11 + S-1群) と、CPT-11 (150mg/m2, day 1) を2週毎に投与する群 (CPT-11群) に、無作為に割り付けられ、増悪するまで投与された (図1)。
本試験は第II相/第III相試験として実施されており、主要評価項目は、第II相試験が6週時点におけるPD例の割合、第III相試験がOSであった。また、副次評価項目は、PFS、TTF (time to treatment failure: 治療成功期間)、奏効率、安全性、3rd-lineへの移行割合であった。
第II相部分は、PD例の割合の閾値60%として、目標症例数は60例であった。第III相試験は、CPT-11 + S-1群、CPT-11群におけるOS中央値をそれぞれ7ヵ月、5ヵ月と想定し、登録期間2年、追跡期間2年、両側α=0.05、検出力80%として、目標症例数は300例 (第II相試験の症例を含む) であった。
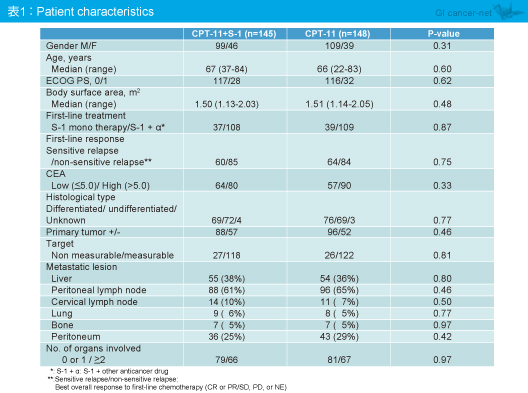
2008年2月〜2011年5月の間に304例が登録され、実際に治療を受けた293例 (CPT-11 + S-1群145例、CPT-11群148例) がFAS (full analysis set) となった。なお、患者背景は両群間で差を認めなかった (表1)。
治療コース中央値は、CPT-11 + S-1群 (3週毎) で4コース、CPT-11群 (2週毎) で6コースであり、使用薬剤の相対用量強度 (RDI) は、CPT-11 + S-1群でCPT-11: 78.3%、S-1: 76.4%、CPT-11群でCPT-11: 80.1%であった。また、PD以外の治療中止の理由は、CPT-11 + S-1群で有害事象 (13.8% vs. 7.4%)、担当医判断 (4.1% vs. 1.4%) が高かった。
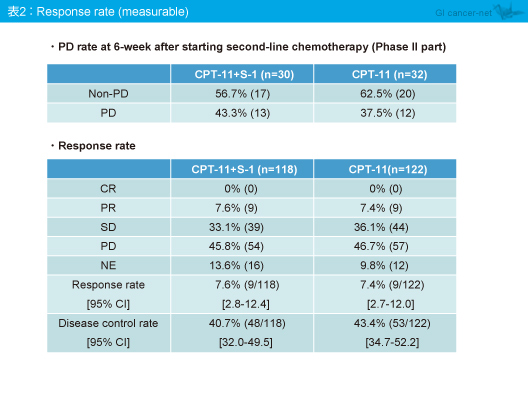
第II相部分の主要評価項目である6週時点のPD例の割合は、CPT-11 + S-1群43.3%、CPT-11群37.5%であった (表2)。また、奏効率は、CPT-11 + S-1群7.6%、CPT-11群7.4%と差はみられなかった。
第II相部分の主要評価項目である6週時点のPD例の割合は、CPT-11 + S-1群43.3%、CPT-11群37.5%であった (表2)。また、奏効率は、CPT-11 + S-1群7.6%、CPT-11群7.4%と差はみられなかった。
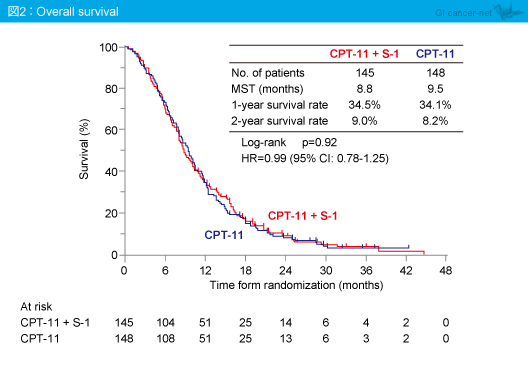
第III相試験の主要評価項目であるOS中央値は、CPT-11 + S-1群8.8ヵ月、CPT-11群9.5ヵ月であり、有意差を認めなかった (HR=0.99, 95% CI: 0.78-1.25, p=0.92) (図2)。
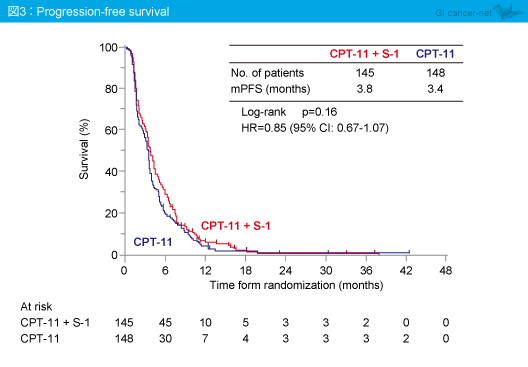
同様に、PFS中央値は、CPT-11 + S-1群3.8ヵ月、CPT-11群3.4ヵ月であり、両群間に有意差を認めず (HR=0.85, 95% CI: 0.67-1.07, p=0.16) (図3)、TTF中央値もそれぞれ3.1ヵ月、3.2ヵ月であり、有意差を認めなかった (HR=0.98, 95% CI: 0.78-1.23, p=0.84)。
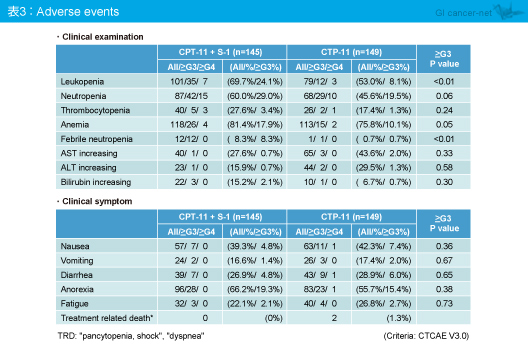
有害事象は、CPT-11 + S-1群で血液毒性が高く、白血球減少 (p<0.01)、貧血 (p=0.05)、発熱性好中球減少症 (p<0.01) が有意に高率であった (表3)。
3rd-lineへの移行割合は、CPT-11 + S-1群62.8%、CPT-11群69.6%であり、差を認めなかった (p=0.22)。なお、3rd-lineで使用された化学療法の約半数はPaclitaxelであり、CPT-11 + S-1群の8.3%、CPT-11群の22%で、Docetaxel/CDDP + S-1が使用されていた。
S-1に治療抵抗性となった進行・再発胃癌に対する2nd-lineとしてのCPT-11 + S-1併用療法は、OSの有意な延長を認めなかった。切除不能進行・再発大腸癌の化学療法では、フッ化ピリミジン系製剤の継続的な使用による有効性が示唆されているが、進行・再発胃癌におけるS-1の継続使用の有効性は示されなかった。
Reference
1) Ueda S, et al.: 2012 Annual Meeting of the American Society of Clinical Oncolagy®: abst #4002
2) Koizumi W, et al.: Lancet Oncol. 9(3): 215-221, 2008[PubMed]
3) Sugimoto N, et al.: Gan To Kagaku Ryoho. 36(3): 417-424, 2009[PubMed]
4) Yamada Y, et al.: Int J Clin Oncol. 8(6): 374-380, 2003[PubMed]
1) Ueda S, et al.: 2012 Annual Meeting of the American Society of Clinical Oncolagy®: abst #4002
2) Koizumi W, et al.: Lancet Oncol. 9(3): 215-221, 2008[PubMed]
3) Sugimoto N, et al.: Gan To Kagaku Ryoho. 36(3): 417-424, 2009[PubMed]
4) Yamada Y, et al.: Int J Clin Oncol. 8(6): 374-380, 2003[PubMed]
