
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
20050181試験におけるKRAS /NRAS 変異の解析:切除不能進行・再発大腸癌の2nd-lineにおけるPanitumumab + FOLFIRI vs. FOLFIRIの第III相試験
Analysis of KRAS /NRAS Mutations in the Phase 3 20050181 Study of Panitumumab + FOLFIRI vs. FOLFIRI as Second-line Treatment for Metastatic Colorectal Cancer
Marc Peeters, et al.

抗EGFR抗体薬の最適治療ラインは1st-lineか?

本解析の結果は、1st-lineの試験 (PRIME試験、PEAK試験、FIRE-3試験) でRAS 野生型において抗EGFR抗体薬併用群で大きなOS延長が示されたことと比較すると、変異測定部位を広げることによるメリットがやや小さい印象である。抗EGFR抗体薬の効果を最大限発揮するためには、1st-lineの前にKRAS /NRAS 遺伝子変異の有無を明らかにし、野生型の場合には1st-lineから抗EGFR抗体薬併用療法を行う戦略がより適切なのかもしれない。ディスカッサントの指摘どおり、本年の米国臨床腫瘍学会で明らかになるCALGB80405試験の結果がますます切望される状況となったのは間違いない。
RAS による効果予測のエビデンスが確立

総じて、治療ラインの違いを超えて、効果予測因子としてのRAS のエビデンスは確立されたと言える。ただし、1st-lineでのRAS 野生型におけるPanitumumab併用群のOSは、化学療法単独群に比べて、MSTで約6ヵ月 (=26.0−20.2ヵ月) の延長がみられている。このインパクトが大きかった分、今回の2nd-lineの結果は比較的想定内であったという印象は受ける。1st-lineを対象としたFIRE-3試験やPEAK試験でも、RAS 野生型における抗EGFR抗体薬のOS延長効果が予想を超えてBevacizumabを上回っていた。今回の結果を含むRAS のエビデンスは、抗EGFR抗体薬を使用するベストな治療ラインに関する考え方に影響を及ぼすだろう。
KRAS exon 2変異の有無は、切除不能進行・再発大腸癌症例に対する抗EGFR抗体薬投与時の効果予測因子として確立されている1-4)。最近、1st-lineの臨床試験であるPRIME試験やPEAK試験のバイオマーカー解析の結果から、KRAS exon 2のみならず、KRAS exon 3, 4、NRAS exon 2, 3, 4変異の有無がPanitumumabの効果予測因子になることが報告された5, 6)。また、20020408試験も含め、Panitumumabの臨床試験におけるRAS 解析が実施されている。
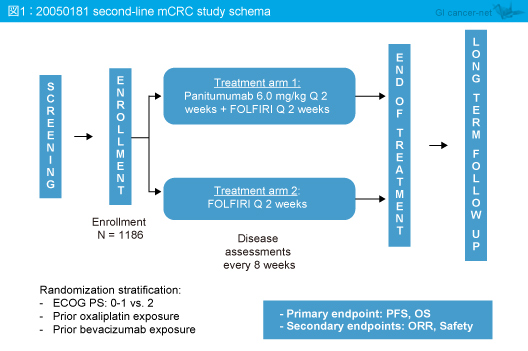
20050181試験は、1st-lineでフッ化ピリミジン系製剤を含む治療に不応となった切除不能進行・再発大腸癌患者を対象に、2nd-lineとしてPanitumumab + FOLFIRI群とFOLFIRI群に割り付けられ、有効性、安全性について検討された (図1)。主要評価項目はPFS、OSであり、副次評価項目は奏効率、安全性であった。
今回の検討は、20050181試験の初回解析結果を元に、RAS 変異の有無 (KRAS exon 2, 3, 4、NRAS exon 2, 3, 4) による有効性を評価することである。なお、RAS 変異は標準法とされているサンガー法とWAVE-based SURVEYOR® Scan Kitsを用いて評価した。対立遺伝子変異と解析方法は事前に明記されており、検査施設では割り付けおよび治療結果は盲検化された。
今回の検討は、20050181試験の初回解析結果を元に、RAS 変異の有無 (KRAS exon 2, 3, 4、NRAS exon 2, 3, 4) による有効性を評価することである。なお、RAS 変異は標準法とされているサンガー法とWAVE-based SURVEYOR® Scan Kitsを用いて評価した。対立遺伝子変異と解析方法は事前に明記されており、検査施設では割り付けおよび治療結果は盲検化された。
20050181試験に登録された1,186例中1,008例 (85%) が今回の解析対象となった。遺伝子変異は、KRAS exon 2 (codon 12, 13) 44.9%、exon 3 (codon 59, 61) 4.4%、exon 4 (codon 117, 146) 7.7%、NRAS exon 2 (codon 12, 13) 2.2%、exon 3 (codon 59, 61) 5.6%、exon 4 (codon 117, 146) 0%であり、KRAS exon 2野生型の18%に何らかのRAS 変異を有していた (図2)。

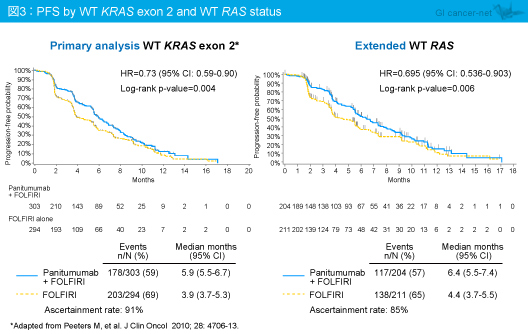
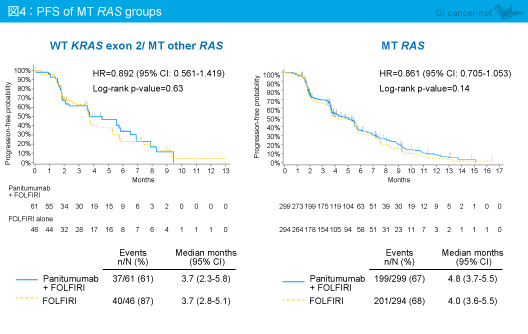
全てのRAS 遺伝子が野生型 (RAS 野生型) におけるPFS中央値は、Panitumumab + FOLFIRI群6.4ヵ月、FOLFIRI群4.4ヵ月であり、KRAS exon 2野生型と同様にPanitumumab + FOLFIRI群で有意に延長した (HR=0.695, 95% CI: 0.536-0.903, p=0.006) (図3)。一方、KRAS exon 2野生型で他のRAS 変異型、あるいはKRAS exon 2を含む何らかのRAS 遺伝子が変異型 (RAS 変異型) では、Panitumumab + FOLFIRI群とFOLFIRI群との間に差はみられなかった (図4)。
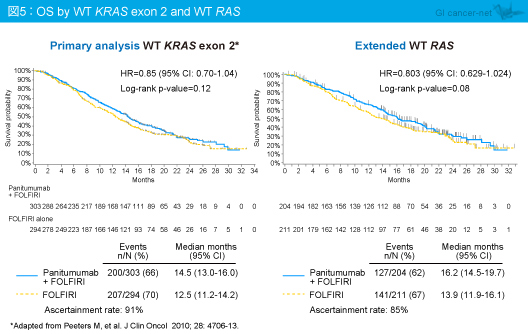
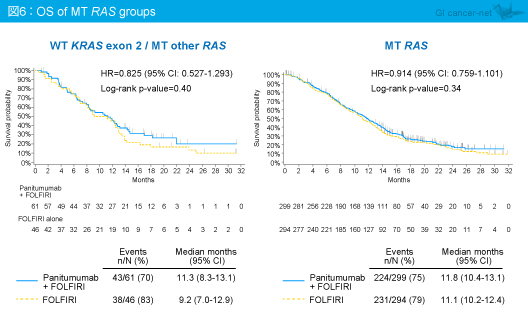
RAS 野生型のOS中央値は、Panitumumab + FOLFIRI群16.2ヵ月、FOLFIRI群13.9ヵ月であり、有意差を認めなかった (HR=0.803, 95% CI: 0.629-1.024, p=0.08) (図5)。また、KRAS exon 2野生型で他のRAS 変異型、あるいはRAS 変異型では、Panitumumab + FOLFIRI群とFOLFIRI群との間に差はみられなかった (図6)。
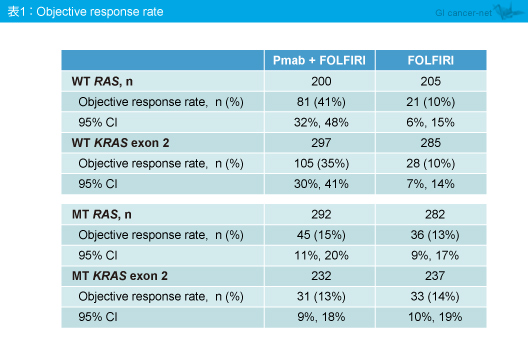
奏効率は、RAS 野生型ではPanitumumab + FOLFIRI群41%、FOLFIRI群10%であり、KRAS exon 2野生型では、Panitumumab + FOLFIRI群35%、FOLFIRI群10%と、いずれも顕著な差がみられたが、RAS 変異型およびKRAS exon 2変異型では両群で同程度であった (表1)。
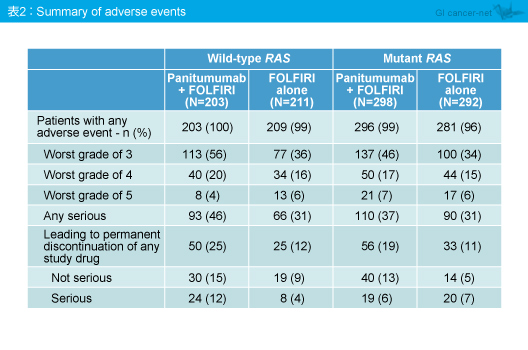
RAS 野生型のPanitumumab + FOLFIRI群における有害事象は既報のKRAS exon 2野生型と大きな差を認めず、新たな有害事象も認めなかった (表2)。
今回、全体解析の85%でRAS 解析を行い、KRAS exon 2野生型におけるRAS 変異型の割合は18%であった。既報のKRAS exon 2野生型と比較すると、RAS 野生型ではPFS、OSともに優れる傾向を示した。一方、RAS 変異型はKRAS exon 2変異型と同様に、FOLFIRIに対するPanitumumabの上乗せ効果を認めなかった。これらの結果から、切除不能進行・再発大腸癌患者へのPanitumumab投与の適正を検討する上でRAS 検査は有用であると言える。
Reference
1) Amado RG, et al.: J Clin Oncol. 26(10): 1626-1634, 2008 [PubMed]
2) Douillard JY, et al.: J Clin Oncol. 28(31): 4697-4705, 2010 [PubMed]
3) Peeters M, et al.: J Clin Oncol. 28(31): 4706-4713, 2010 [PubMed]
4) Van Cutsem E, et al.: N Engl J Med. 360(14): 1408-1417, 2009 [PubMed]
5) Douillard JY, et al.: N Engl J Med. 369(11): 1023-1034, 2013 [PubMed]
6) Karthaus M, et al.: ESMO 2013: abst 2262 [学会レポート]
1) Amado RG, et al.: J Clin Oncol. 26(10): 1626-1634, 2008 [PubMed]
2) Douillard JY, et al.: J Clin Oncol. 28(31): 4697-4705, 2010 [PubMed]
3) Peeters M, et al.: J Clin Oncol. 28(31): 4706-4713, 2010 [PubMed]
4) Van Cutsem E, et al.: N Engl J Med. 360(14): 1408-1417, 2009 [PubMed]
5) Douillard JY, et al.: N Engl J Med. 369(11): 1023-1034, 2013 [PubMed]
6) Karthaus M, et al.: ESMO 2013: abst 2262 [学会レポート]
