
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
切除不能進行・再発大腸癌に対するBevacizumab併用化学療法による導入療法後の維持療法としてのCapecitabine + Bevacizumab vs. 無治療経過観察の比較: Dutch Colorectal Cancer Group (DCCG) による第III相試験CAIRO3試験の最終報告とサブグループ解析
Maintenance Treatment with Capecitabine + Bevacizumab versus Observation after Induction Treatment with Chemotherapy + Bevacizumab in Metastatic Colorectal Cancer: Final Results and Subgroup Analyses of the Phase 3 CAIRO3 Study of the Dutch Colorectal Cancer Group (DCCG)
Miriam Koopman, et al.

Capecitabine + Bevacizumabによる維持療法の有用性を再確認:CAIRO3試験の最終解析結果

本会ではCAIRO3試験の最終解析が報告されたが、主要評価項目であるCAPOX + Bevacizumab療法再導入後の増悪までの期間 (PFS2) については、2013年米国臨床腫瘍学会の報告と同様に、維持療法の有効性 (維持療法群11.7ヵ月、経過観察群8.5ヵ月; HR=0.67, p<0.0001) が報告されたが、副次評価項目のOSに関しては今回も有意差を示すことはできなかった。
なお本会では、事前に規定された各因子によるサブグループ解析が示され、PFS2に関しては全ての因子において維持療法に良好な傾向が認められたが、OSに関してはいくつかの因子において維持療法による有効性は示されなかった。あくまでもサブグループ解析であるが、同対象のなかに維持療法が不要な症例が存在している可能性を示唆する結果であった。可能であればMACRO試験2) やOPTIMOX試験1,3) などとの統合解析を行い、Chemo-free intervalを選択できる症例を探索する、さらなる検討を切望する。
CAIRO3試験は切除不能進行・再発大腸癌に対するCapecitabine (Cap) + L-OHP + Bev (CAPOX-B) 療法による導入療法で増悪のない患者を対象として、維持療法としてのCap + Bev療法と経過観察を比較検討した第III相試験である。
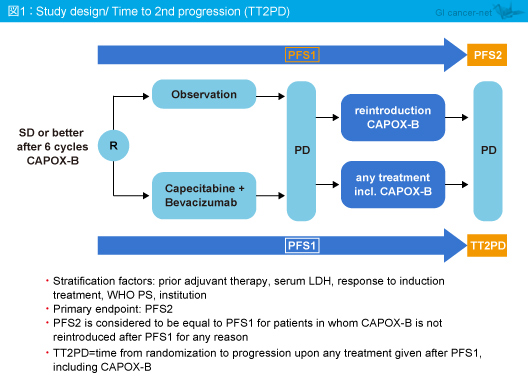
対象はPS 0-1の切除不能進行・再発大腸癌患者であり、初回導入療法としてCAPOX-B療法6サイクル後SD以上の患者について、経過観察群と維持療法群 (Cap + Bev) に無作為に割り付けられた (図1)。両群ともに無作為化してから初回PD (PFS1) 後にCAPOX-B療法を再導入し、2回目のPD (PFS2) となるまで継続した。なお、PFS1は「無作為化から初回PDまでの期間」、PFS2は「無作為化から2回目のPDまでの期間」とし、CAPOX-B療法を再導入できなかった患者はPFS1 = PFS2とした。PFS2が9ヵ月から11.5ヵ月に延長すると仮定し (ハザード0.78)、検出力80%、両側α=0.05で、必要イベント数は525であった。
主要評価項目はPFS2であり、副次評価項目はOS、TT2PD (PFS1後に受けた全ての治療における2回目のPDまでの期間)、QOLであった。また、その他いくつかのサブグループ解析が事前に計画されていた。
主要評価項目はPFS2であり、副次評価項目はOS、TT2PD (PFS1後に受けた全ての治療における2回目のPDまでの期間)、QOLであった。また、その他いくつかのサブグループ解析が事前に計画されていた。
オランダの74施設から558例が登録され、経過観察群279例、維持療法群279例に割り付けられた。また、観察期間中央値は48ヵ月であった。
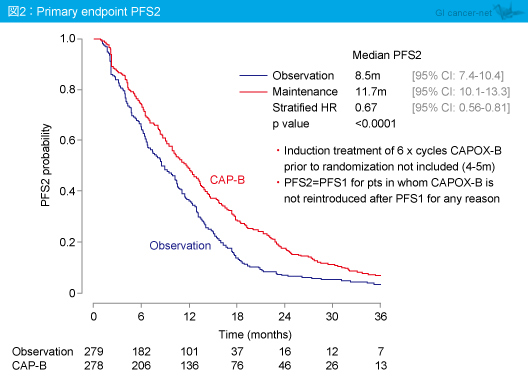
PFS1中央値は、経過観察群4.1ヵ月、維持療法群8.5ヵ月 (HR=0.43, 95% CI: 0.36-0.52, p<0.0001)、主要評価項目のPFS2中央値は経過観察群8.5ヵ月、維持療法群11.7ヵ月であり (HR=0.67, 95% CI: 0.56-0.81, p<0.0001) (図2)、ともに有意差が認められた。
PFS1中央値は、経過観察群4.1ヵ月、維持療法群8.5ヵ月 (HR=0.43, 95% CI: 0.36-0.52, p<0.0001)、主要評価項目のPFS2中央値は経過観察群8.5ヵ月、維持療法群11.7ヵ月であり (HR=0.67, 95% CI: 0.56-0.81, p<0.0001) (図2)、ともに有意差が認められた。
PFS1から2回目のPDまでの治療において、CAPOX-B療法の再導入は経過観察群60%、維持療法群48%で実施された。CAPOX-B療法を再導入できなかった患者は経過観察群37% (103例)、維持療法群48% (134例) であり、これらの症例はCap/5-FU + Bev、CPT-11、抗EGFR抗体薬療法などで治療されていた。
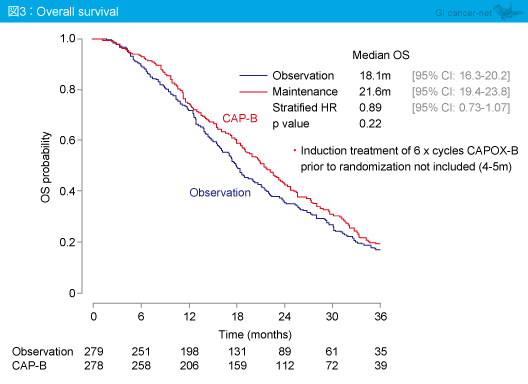
TT2PD中央値は、経過観察群11.1ヵ月、維持療法群13.9ヵ月であり、維持療法群で有意な延長が認められた (HR=0.68, 95% CI: 0.57-0.82, p<0.0001)。一方、OS中央値は経過観察群18.1ヵ月、維持療法群21.6ヵ月であり、有意差は認められなかった (HR=0.89, 95% CI: 0.73-1.07, p=0.22) (図3)
TT2PD中央値は、経過観察群11.1ヵ月、維持療法群13.9ヵ月であり、維持療法群で有意な延長が認められた (HR=0.68, 95% CI: 0.57-0.82, p<0.0001)。一方、OS中央値は経過観察群18.1ヵ月、維持療法群21.6ヵ月であり、有意差は認められなかった (HR=0.89, 95% CI: 0.73-1.07, p=0.22) (図3)
QOLは経過観察群と維持療法群に3.9%の差がみられたが (95% CI: 1.2-6.5, p=0.004)、10%未満のため臨床的な差と判定されなかった。
OSの多変量解析によるサブグループ解析において、無作為化前の初回導入療法 (CAPOX-B療法) に対する奏効例 (CR/PR)、同時性病変に対する原発巣切除例では、維持療法群の有用性がみられた (図4)。なお、PFS1、PFS2、TT2PDはサブグループ解析において、維持療法の有用性が確認された。
OSの多変量解析によるサブグループ解析において、無作為化前の初回導入療法 (CAPOX-B療法) に対する奏効例 (CR/PR)、同時性病変に対する原発巣切除例では、維持療法群の有用性がみられた (図4)。なお、PFS1、PFS2、TT2PDはサブグループ解析において、維持療法の有用性が確認された。
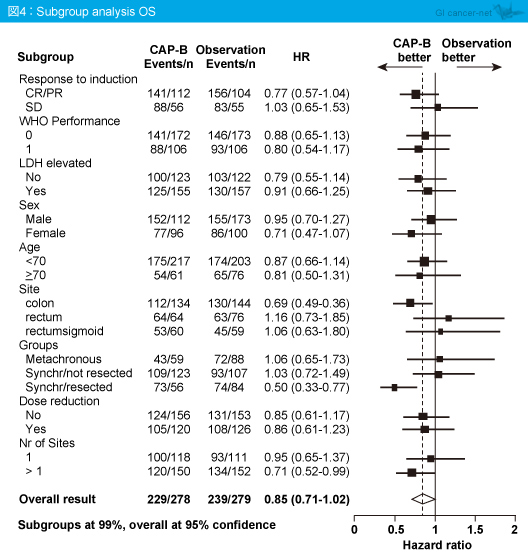
CAIRO3試験の全体の解析およびサブグループ解析において、PFS1、PFS2、TT2PDについて維持療法の有用性は確認された。OSについては、全体の解析において維持療法の有用性は認められなかったが、初回導入療法への奏効例や同時性病変に対する原発巣切除例のサブグループにおいてはOSに対する維持療法の有用性が認められた。
Reference
1) Buyse M, et al.: ESMO2006: abst #329O
2) Tabernero J, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®: abst #3501
3) Chibaudel B, et al.: J Clin Oncol. 27 (34): 5727-5733, 2009[PubMed]
1) Buyse M, et al.: ESMO2006: abst #329O
2) Tabernero J, et al.: 2010 Annual Meeting of the American Society of Clinical Oncology®: abst #3501
3) Chibaudel B, et al.: J Clin Oncol. 27 (34): 5727-5733, 2009[PubMed]
