
|
このサイトは医療関係者の方々を対象に作成しています。必ずご利用規約に同意の上、ご利用ください。記事内容で取り上げた薬剤の効能・効果および用法・用量には、日本国内 で承認されている内容と異なるものが、多分に含まれていますのでご注意ください。 |
手術未施行食道癌に対するPaclitaxel + Cisplatin + 放射線療法へのCetuximabの上乗せ効果を検討した第III相試験:RTOG0436試験の初回報告
The Initial Report of RTOG 0436: A Phase III Trial Evaluating the Addition of Cetuximab to Paclitaxel, Cisplatin, and Radiation for Patients with Esophageal Cancer Treated without Surgery
Mohan Suntharalingam, et al.

食道癌に対する化学放射線療法にCetuximab併用は無効

今回報告されたRTOG0436試験は局所進行食道癌を対象に、化学放射線療法 (Paclitaxel + Cisplatin(CDDP) + 放射線療法50.4Gy) に対するCetuximabの上乗せ効果を検証した第III相試験である。しかし、結果は残念ながらCetuximab併用による生存期間の延長は示せず、内視鏡判定による臨床的完全奏効 (cCR) の割合を増やすこともできなかった。残念ながら本会の発表では組織診断別の生存解析は報告されなかったが、食道癌で主体となる扁平上皮癌のサブセットでもcCRの改善は示せず、頭頸部癌とは乖離した結果となった。
上記2つの試験結果を鑑みると、現時点で食道癌の化学放射線療法におけるCetuximab併用の有用性は否定せざるを得ない。しかし、本試験では85%の組織検体が回収されているとのことであり、バイオマーカー解析により有効例を囲い込めるかどうかにわずかな期待を寄せたい。
切除不能な局所進行食道癌に対する標準治療は化学放射線療法である。RTOG0436試験は、手術未施行の食道癌に対するPaclitaxel + CDDP + 放射線療法へのCetuximabの上乗せ効果を検討する無作為化第III相試験であり、今回、初回中間解析の結果を報告する。
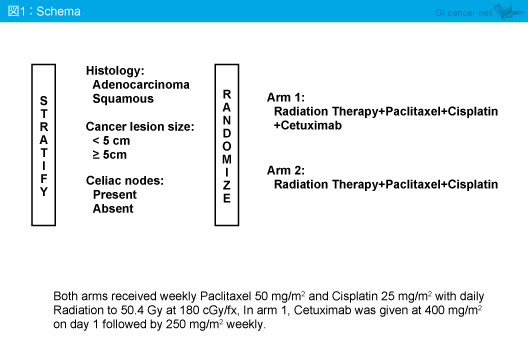
対象は18〜75歳、Zubrod PS 0-2で組織学的に食道の扁平上皮癌または腺癌と診断され、AJCC 2002病期分類におけるT1N1M0、T2-4/any N/M0、any T/any N/M1aの症例とし、化学放射線療法を施行する群 (RT + Chemo群) と化学放射線療法にCetuximab併用群 (RT + Chemo + Cetuximab群) とに無作為に割り付けられた。また、組織診断別 (腺癌 vs. 扁平上皮癌) 、腫瘍サイズ (5cm未満 vs. 5cm以上) 、腹腔リンパ節転移の有無で層別化された (図1)。化学放射線療法は、Paclitaxel (50mg/m2, weekly) + CDDP (25mg/m2, weekly) + 放射線療法 (総線量50.4Gy, 1.8Gy/回×28日) であり、RT + Chemo + Cetuximab群はCetuximab (初回400mg/m2 以降250mg/m2, weekly) を追加投与した。
主要評価項目はOSとし、副次評価項目は局所コントロール (cCRの増加および局所再発の低下) 、有害事象、内視鏡的奏効率などであった。Cetuximab併用により2年OSが41%から53%に改善されると仮定し (HR=0.71) 、検出力80%、片側α=0.025で目標症例数420例 (OSイベント数281) とした。また、組織診断別によるcCRの中間解析は、Cetuximab併用によりcCRが40%から52%に改善されると仮定し、検出力84%、片側α=0.10で、組織診断別に最初の150例において行われた。
主要評価項目はOSとし、副次評価項目は局所コントロール (cCRの増加および局所再発の低下) 、有害事象、内視鏡的奏効率などであった。Cetuximab併用により2年OSが41%から53%に改善されると仮定し (HR=0.71) 、検出力80%、片側α=0.025で目標症例数420例 (OSイベント数281) とした。また、組織診断別によるcCRの中間解析は、Cetuximab併用によりcCRが40%から52%に改善されると仮定し、検出力84%、片側α=0.10で、組織診断別に最初の150例において行われた。
2008年6月に目標症例数420例で登録が開始されたが、2013 Gastrointestinal Cancers SymposiumでSCOPE1試験の結果が発表されたため、2013年1月までに登録された344例が対象となった。344例中328例 (RT + Chemo + Cetuximab群159例、RT + Chemo群169例) で解析可能であり、患者背景は両群でバランスがとれていた。
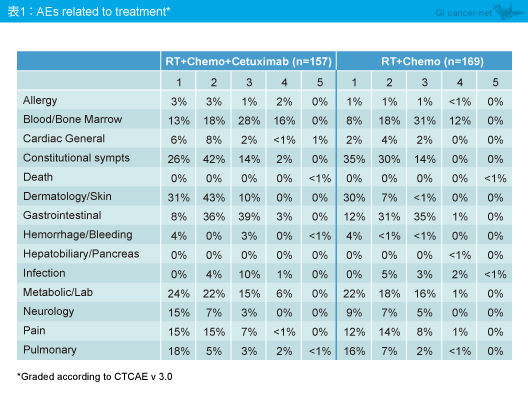
治療関連有害事象は、RT + Chemo + Cetuximab群で皮膚障害の頻度が高かったが、それ以外は両群に大きな差はみられなかった (表1)。
治療関連有害事象は、RT + Chemo + Cetuximab群で皮膚障害の頻度が高かったが、それ以外は両群に大きな差はみられなかった (表1)。
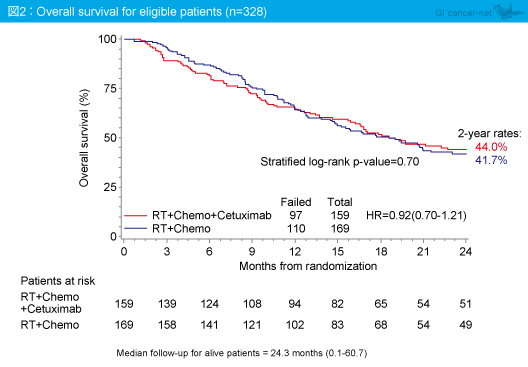
生存例の追跡期間中央値24.3ヵ月時における2年OSはRT + Chemo + Cetuximab群44.0%、RT + Chemo群41.7%であり、両群間に有意差を認めなかった (HR=0.92, 95% CI: 0.70-1.21, p=0.70) (図2)。
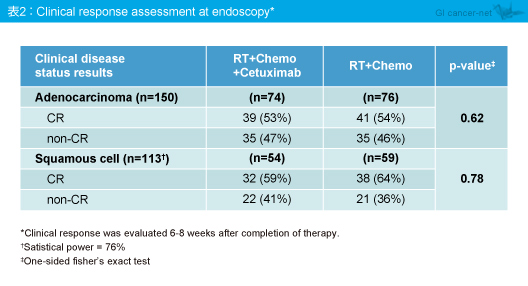
OSにおける多変量解析では、PS 0 (vs. 1/2) (HR=1.56, p=0.0015) および腫瘍サイズ5cm未満 (vs. 5cm以上) (HR=1.72, p=0.0002) においてOSが有意に良好であった。また、内視鏡判定によるcCRは、腺癌 (p=0.62) 、扁平上皮癌 (p=0.78) ともにCetuximab併用による上乗せ効果はみられなかった(表2)。
なお、cCR達成例は残存病変例に比べOSが有意に良好であり (HR=2.12, 95% CI: 1.59-2.83) 、腺癌 (HR=1.59, 95% CI: 1.11-2.26) 、扁平上皮癌 (HR=3.67, 95% CI: 2.22-6.07) のいずれにおいても有意差が認められた。
化学放射線療法に対するCetuximabによるOSの改善は認められず、cCRも組織診断別にかかわらず改善されなかった。また、治療後6〜8週間にcCRを達成した症例は有意に2年OSを延長し、PSと腫瘍サイズはOSの有意な効果予測因子となった。これらの知見は、非選択的な患者に対する切除を伴わない化学放射線療法に現在使用可能なEGFR阻害剤を加えてもOSは改善されないという、これまでのエビデンスを補強するものである。
