 |
 |
| �͂��߂� / �݊��ɑ���V�K�R����
/ �ŋ߂̓����ɂ��� |
| �͂��߂� |
| |
�@2001�N3�����s�w�݊����ÃK�C�h���C���x1)�̂Ȃ��Ɂu�ŋ߁A�t�����̍�����܁A���邢�͕��p�Ö@������Ă���B�������A�����ɋ�������p�����Ƃ�����̂ŁA����p�ɑ���K�ȑΉ����K�v�ł���B(�㗪)�v�Ƃ̋L�ڂ�����B����docetaxel(TXT)�Apaclitaxel(TXL)�Airinotecan(CPT-11)�Alevofolinate/fluorouracil(l-LV/5-FU)�ATS-1�Ȃǂ́A�݊����ÂɎg���n�߂����ł���A�m����f�[�^�͑��݂��Ȃ������B�������A�����̊w��ł͂�����܂̗L�p������������A���ł͈݊����w�Ö@�̑I���������I�ɍL���Ă���B
�@�{�e�ł͑�75��݊��w��(2003�N)�́u�݊����Âɂ�����V�K�R���܁v�Ƃ����V���|�W�E���łƂ肠����ꂽ�V�K�R���܂𒆐S�ɍŋ߂̓������T������B |
| |
�����̃y�[�W�̃g�b�v�� |
| �݊��ɑ���V�K�R���� |
| |
levofolinate/fluorouracil(l-LV/5-FU)
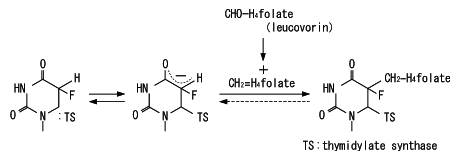
�@l-LV���̂��̂ɂ͍R��ᇌ��ʂ͂Ȃ����A5-FU�̍R��ᇌ��ʂ�����ړI�Ŏg����biochemical modulation�̘_�������p�������w�Ö@�ł���BLV��d�̂�l�̂�����diastereomer�ł��邪����������l�݂̂̂ɂ���A�A�C�\�{����®��l�݂̂̂𒊏o������܂ł���B
�@5-FU�̑�ӕ��ł���FdUMP��6�ʂ�TS(thymidylate synthase)��������TS�����������邪�A���̌����͔L�����ł���キ����₷���B�������AFdUMP��5�ʂ�CH2FH4(5,10-methylene
tetrahydrofolate)�����������ꍇ�AFdUMP�ATS�ACH2FH4�̎O�҂͋��͂Ɍ������ATS�����̑j�Q�����������B����CH2FH4���������邽�߂�l-LV�𓊗^����(�}1)�B
�@���̕��p�Ö@�̓��{�z���i�[�g�E�t���I���E���V���Ö@(l-LV/5-FU�Ö@)�Ə̂���A�ʏ�A���l�ɂ�l-LV 250mg/m2/���2���Ԃ����ē_�H�Ò�����Bl-LV�̓_�H�Ò��J�n1���Ԍ��5-FU
600mg/m2/���3���ȓ��Ŋɏ��ɐÒ����A1�T�Ԃ��Ƃ�6��J��Ԃ�����A2�T�ԋx��B�����1�N�[���Ƃ��Ă���B
�@l-LV��1999�N10���ɔ�������A�݊��ɑ���t������29.8��(50/168��)�ł���A��ȕ���p�͔����������A�����A�H�~�s�U�A���S�E�q�f�Ȃǂł���B
�@���Ăł�Petrelli2)�AMachover3)�AO�fConnell4)��ɂ���đ咰���ɑ���D�ꂽ���ʂ�����Ă���A�W�����ÂƂ���Ă��邽�߁A�{�M�ł��咰�����Âɉ��p����邱�Ƃ������B
�@�݊����Âɂ����Ă�CDDP5)��etoposide6)�Ƃ̕��p�ɂ����ʑ�����MST(median survival
time)�̉���������Ă��邪�A�����taxan�n�R���܂�CPT-11�ȂǂƂ̕��p�ɂ��L�p�����オ���҂����B |
| �}1. l-LV/5-FU�Ö@�̍�p�@�� |
| |
 |
| |
�����̃y�[�W�̃g�b�v�� |
| |
irinotecan(CPT-11)
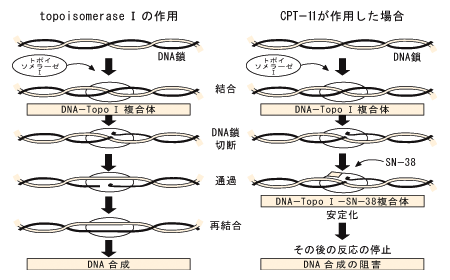
�@�����Y����ȂǂɊ܂܂��camptothecin�̔������U���̂ł���CPT-11�́A1995�N�Ɉ݊��̓K����lj����Ă���B���̍�p�@����CPT-11�̊�����ӕ��ł���SN-38���T�^DNA
topoisomerase�̍�p��j�Q���ADNA�̍�����j�Q���邱�Ƃɂ��E�זE���ʂ�����(�}2)�B
�@�݊��ɂ�A�@(�ʏ�A���l��1��1��ACPT-11 100mg/m2��1�T�ԊԊu��3�`4��_�H�Ò����A���Ȃ��Ƃ�2�T�ԋx��)��B�@(�ʏ�A���l��1��1��ACPT-11
150mg/m2��2�T�ԊԊu��2�`3��_�H�Ò����A���Ȃ��Ƃ�3�T�ԋx��)��2�ʂ�̎��Ö@������BA�@��B�@�ɂ������II�������̐��т�\1�Ɏ������A�����̐��т��F�߂��Ă���7)�B
�@��ȕ���p�́A�P�܂͂�����p�Ö@�ł��A����������(���ɍD��������)�≺������������Ă���B�����ɂ͖{�܂̃R�����쓮���ɂ���ߐ��̑����^�ƁA������ӕ�SN-38�ɂ��x���^�Ƃ�����B
�@�݊����Âɂ�5-FU�Ȃǂ̑�ӝh�R�܂�CDDP�Ȃǂ̔������܂������g����̂ŁA�����I�ȍ�p�@��������CPT-11�͑��܂ƕ��p���鉿�l�͍����B��75��݊��w��ɂ�����CPT-11�̕��p��܂�CDDP����ԑ��������B�܂��ACPT-11��5-FU�̎E�זE��p�ɂ�����key
enzyme�ł���TS�̊������������p������A5-FU�n�R���܂Ƃ̕��p�͘_���I�ɂ��Ӌ`������ƍl������(�\2)8)�B |
| �}2. CPT-11�ɂ��I�^DNA topoisomerase�̑j�Q |
| |
 |
| |
|
�\1. CPT-11�����II�������̍R��ᇌ���
(�Ō`���w�Ö@���ڌ��ʔ����A�݊��戵���K��ɂ��) |
| |
 |
| ���^�@ |
�K�i�� |
���S�� |
CR |
PR |
MR |
NC |
PD |
�t����
�i�K�i��j |
95���M����� |
| |
76 |
60 |
0 |
14 |
4 |
23 |
19 |
18.4�� |
9.7-27.1�� |
| A�@ |
38 |
28 |
0 |
7 |
1 |
10 |
10 |
18.4�� |
|
| B�@ |
38 |
32 |
0 |
7 |
3 |
13 |
9 |
18.4�� |
|
|
 |
|
| |
|
| �\2. 5-FU�ACPT-11�P�Ƃ���ѕ��p����HT-29�ɂ�����thymidylate
synthase���� |
 |
| |
thymidylate
synthase�ipmol/min/mg protein , mean�}SD�j |
| |
���ԁi�����j |
| ��ܖ� |
0 |
24 |
48 |
72 |
96 |
| controls |
2.8�}1.6 |
|
|
|
|
| 5-FU |
|
0.052�}0.047 |
0.048�}0.05 |
0.075�}0.037 |
0.135�}0.061 |
| CPT-11 |
|
2.91�}0.96 |
1.43�}0.59 |
1.85�}0.28 |
|
| CPT-11�{5-FU�iCPT-11��s�j |
|
2.91�}0.96 |
0.057�}0.075 |
0.021�}0.0068* |
0.033�}0.02* |
| 5-FU�{CPT-11�i5-FU��s�j |
|
0.052�}0.047 |
0.053�}0.038 |
0.046�}0.023 |
|
| 5-FU�{CPT-11�i�����j |
|
0.040�}0.009 |
0.053�}0.031 |
0.062�}0.048 |
|
|
 |
5 - FU�����CPT - 11���e�X��IC5 0�Ńq�g��������HT-29��24���ԐڐG�������B
�l��3��̎������ʂ̕��ϒl�}SD�������B
*�Fp��0.05�ivs. 5 -FU�j |
 |
|
| |
docetaxel(TXT)
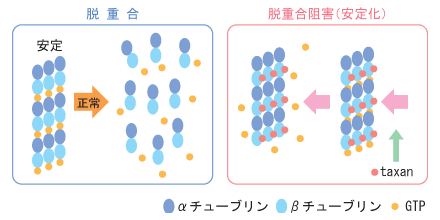
�@TXT�����TXL(��q)�͂Ƃ���taxan�Ə̂���A�זE���̔����ǂɍ�p�����܂ł���B�����ǂ̓�����у��`���[�u�����̓�ʑ̂̏d���ł��邪�Ataxan�̓`���[�u���������𑣐i�E���艻���A�E�d����}�����邱�Ƃɂ��זE�����j�Q���A�R��ᇌ��ʂ�����(�}3)�B
�@TXT��2000�N4���Ɉ݊��̓K����lj����A�t������17.1��(22/129��)�ł���B�ʏ�A���l��1��1��ATXT60mg/m2��1���Ԉȏォ����3�`4�T�ԊԊu�œ_�H�Ò�����B1��ō��p�ʂ�70mg/m2�ł���B�ŋ߂͕���p�y���̖ړI��1�^�ʂ�30�`40mg/m2�Ƃ���weekly���邢��biweekly���^�����݂��Ă���B
�@��ȕ���p�͍D���������A�E�сA�H�~�s�U�ȂǂŁA���ٓI�Ȃ��̂Ƃ��Ė{�܊ܗL�̓Y�����ł���|���\���x�[�g80������ƂȂ�ߕq�ǂ�����B�܂��A�����̍o�t�����������I�ȕ���p�ł��邪�A�{�M�ł�1�^�ʂ�60mg/m2�Ə��Ȃ����߂��܂���ɂȂ邱�Ƃ͂Ȃ��Bin
vitro�ł�5-FU�ACDDP�Aetoposide�ƌ����ϐ���F�߂Ȃ�9)���߁A�����̖�܂Ƃ̕��p��2nd line�Ƃ��Ă̗L�p������������Ă���B |
| �}3. taxan�̍�p�@�� |
| |
 |
| |
�����̃y�[�W�̃g�b�v�� |
| |
paclitaxel(TXL)
�@TXL��taxan�̈��ł��邪�ATXT�ƈقȂ������HSR(hypersensitivity reaction)���F�߂���_�ł���B�����TXL���g�ɂ��\�������邪�ATXL���܊ܗL��cremophor
EL �����������Ńq�X�^�~����V�����ߕq�������N�������Ƃ���Acremophor EL�����̎���ƍl������B���������t�玿�X�e���C�h��R�q�X�^�~���܂̑O���^�ɂ��HSR
���}���ł��邽�ߗՏ��I�Ɏx��͂Ȃ��B
�@�݊��̓K����TXT���1�N�x���2001�N5���ɒlj����A�t������23.4��(25/107��)�ł���B�ʏ�A���l��1��1��ATXL 210mg/m2��3���Ԃ����ē_�H�Ò����A���Ȃ��Ƃ�3�T�ԋx�邱�ƂɂȂ��Ă��邪�ATXT�Ɠ��lweekly���邢��biweekly���^����邱�Ƃ������A����1�^�ʂ�70�`80mg/m2�������B
�@��ȕ���p�͍D���������A�E�сA�H�~�s�U�A�����_�o��Q��ؓ��ɂȂǂł���BTXT�Ɠ��l�A���܂Ƃ̌����ϐ����Ȃ��̂ŁA���p��2nd line�Ƃ��Ă̗L�p������������Ă���B
TS-1
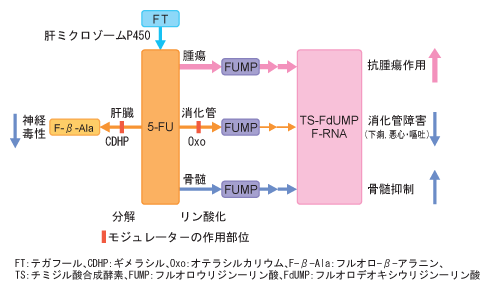
�@TS-1��5-FU��prodrug�ł���tegafur(FT)��gimeracil(CDHP)��oteracil potassium(Oxo)��2��modulator��������1:0.4:1�Ŕz�������o���R������ᇍ܂ł���(�}4)�B
�@���Ȃ킿FT�����ӂ��ꂽ5-FU�̕�����CDHP�ɂ���ė}�����A5-FU�̌�������ю�ᇓ��Z�x�����߁A�����ǂɂ�����5-FU�̃����_����Oxo�ɂ���ė}����������Ǐ�̌y����}������܂ł���B
�@1999�N3���ɔ�������A�t������46.5��(60/129��)�ŁA�P�܂̑t�����͊����̍R���܂̒��ł͂��Ȃ荂�����ł���B�ʏ�A���l�ɂ�TS-1 80mg/m2�A�[�H���1��2��A28���ԘA���o�����^���A���̌�14���ԋx��B�����1�N�[���Ƃ��ČJ��Ԃ��B��ȕ���p�͍����}���A�H�~�s�U�A�����A�F�f�����Ȃǂł���B
�@5-FU������DPD(dihydropyrimidine dehydrogenase)��}�����邱�Ƃɂ��R��ᇌ��ʂ͔���I�Ɍ��シ��BSobrero��10)�͂���DPD�j�Q��p��L���邩�ۂ��ɂ��A5-FU�n�R���܂�DIF(DPD
inhibitory fluoropyrimidine)��non-DIF�ɕ��ނ��Ă���ATS-1��DIF�ɑ�����B
�@���݂͐i�s�E�Ĕ��݊���Ώۂ�TS-1 vs CDDP�{TS-1�̔�r�������s���Ă���B�܂��A�݊��p��Ǘ�ɑ��Ď�p�P�ƌQ��TS-1���^�Q��2�Q�Ԃ�TS-1�̏p��⏕���w�Ö@�ɂ�����L�p���������鎎�����i�s���ł���B |
| �}4. TS-1�̔z�����_ |
| |
 |
| |
�����̃y�[�W�̃g�b�v�� |
| �ŋ߂̓����ɂ��� |
| |
�@2002�����2003�N�ɍs��ꂽ�݊��w�����݂�ƁA�O�q�����R���܂Ɋւ��鉉�肪�ڗ��B�\3�Ɏ����悤�ɉ��w�Ö@�̉����萔�́ATS-1��taxan�������Ȃ��Ă��Ă��邪�A�ˑR�Ƃ���CDDP�������B�܂��R���܂̌����͕��p�Ö@�Ɋւ�����́A�������T/II�������̌��ʕ��䓪���Ă���ATS-1���x�[�X�ɂ������肪�����݂���(�\4)�B
�@���̂ق��A1st line�A2nd line�Ƃ��������ÃX�P�W���[���������������̂������A���^�@�̕ύX�ɂ����ʂ̑�����QOL�̌����ړI�ɁA��������p�Ɋւ��錤���͐���ɂȂ�ƍl������B�܂�Buyse��11)�́A14�J����overall
survival(OS)��B�����郌�W�����ł́A20���ł������t������40���Ɍ��サ���Ƃ��Ă�OS��1.7�J���A60���Ɍ��サ���Ƃ��Ă�3.4�J�������������Ȃ��ƕ��Ă���B�]���Đ������Ԃ�����������@��1st
line�̉��P�ł͂Ȃ��A�K�Ȏ��ɕ�����line��p���邱�Ƃ��̗v�ł���Ƃ�����B�܂�R���v���C�A���X�̍������w�Ö@���D�܂����Ƃ������ƂɂȂ�B
�@��̑O�̈݊����w�Ö@�Ƃ�����mitomycinC(MMC)��5-FU�n��܂����S�ł��������ACDDP�̏o���ɂ��CDDP�{5-FU�n���p�Ö@������Ɏ���đ������B�����č��ATS-1�ACPT-11�Ataxan�����F����A���ꂼ��̕��p����������ɍs���Ă���B�݊����w�Ö@�̑I�������L���������Ƃ͊�������A����͂�����܂̎��Ð��т������ɑ̌n�����R���v���C�A���X�̍����A�������Ԃ̉����Ɋ�^�ł��鎡�ÃX�P�W���[����n�����Ă��������A�����Տ���ɉۂ���ꂽ�Ӗ��ƍl������B |
| �\3. �݊��w���ɂ����鉻�w�Ö@�̉����萔 |
| |
 |
| ��ܖ� |
2002�N |
2003�N |
| TS-1 |
35 |
48 |
| TXL |
6 |
48 |
| CDDP |
27 |
41 |
| TXT |
4 |
17 |
| CPT-11 |
4 |
4 |
| 5-FU |
23 |
14 |
| 5�f-DFUR |
6 |
8 |
| UFT |
4 |
5 |
| ���̑� |
18 |
15 |
|
 |
|
| �\4. �݊��w���ɂ����镹�p���w�Ö@�̉��萔 |
| |
 |
| ���W���� |
2002�N |
2003�N |
| TS-1�{CDDP |
8 |
14 |
| CDDP�{CPT-11 |
4 |
6 |
| CDDP�{TXL |
|
5 |
| TS-1�{TXL |
|
5 |
| TS-1�{TXT |
1 |
4 |
| CDDP�{5FU |
3 |
|
| 5FU�{MTX |
4 |
|
|
 |
|
| |
|
| ������ |
| |
| 1) |
���{�݊��w��ҁF�݊����ÃK�C�h���C����t�p. 2001�N3���ŁA
�����o�ŁAp13,2001 |
| 2) |
Petrelli N,et al.�FA prospective randomized trial of 5-fluorouracil
versus�@5-fluorouracil and high-dose leucovorin versus 5-fluorouracil and methotrexate
in�@previously untreated patients with advanced colorectal carcinoma. J.Clin.Oncol.,5(10)�F1559-1565,1987 |
| 3) |
Machover D,et al.�FTreatment of advanced colorectal and gastric
adenocarcinomas with 5-fluorouracil and high-dose folinic acid. J.Clin.Oncol.,4(5)�F685-696,1986 |
| 4) |
O'Connell MJ�FA phase III trial of 5-fluorouracil and leucovorin
in the treatment of advanced colorectal cancer. A Mayo Clinic/North Central Cancer
Treatment Group study. Cancer,63�F1026-1030,1989 |
| 5) |
���X�؏�Y ���F�؏��s�\�A�Ĕ��݊��ɑ��鉻�w�Ö@
������O��,21(8)�F1317-1325,1998 |
| 6) |
Nakajima T,et al.�FCombined intensive chemotherapy and radical
surgery for incurable gastric cancer. Ann.Surg.Oncol.,4(3)�F203-208,1997 |
| 7) |
��c�؍_�� ���F�Ĕ��E�i�s�݊��ɑ���CPT-11�̌����2���Տ�����
���Ɖ��w�Ö@,21�F1033-1038,1994 |
| 8) |
Guichard S,et al.�FCellular interactions of 5-fluorouracil and
the camptothecin analogue CPT-11(irinotecan)in a human colorectal carcinoma cell
line. Biochem. Pharmacol.,55(5)�F667-676,1998 |
| 9) |
Hill BT,et al.�FDifferential cytotoxic effects of docetaxel in
a range of mammalian tumor cell lines and certain drug resistant sublines in vitro.
Invest.New Drugs,12(3)�F169-182,1994 |
| 10) |
Sobrero A,et al.�FNew directions in the treatment of colorectal
cancer�Fa look to the future. Eur.J.Cancer,36(5)�F559-566,2000 |
| 11) |
Buyse M,et al.�FRelation between tumour response to first-line
chemotherapy and survival in advanced colorectal cancer�Fa meta-analysis. Lancet,356
(9227)�F373-378,2000 |
|
| |
2003�N7�����s |

