 |
3年DFSは5年OSから7年OSの代替エンドポイントへ |
|
 |
|
| 坂本: 昨日、de Gramont先生が「再発結腸癌患者の再発後の生存期間が1年から2年に延長され、3年DFSと5年OSの相関が弱まり、6年OS・7年OSとの強い相関が認められた」と報告されました。こちらについて、先生のご意見をおうかがいできますか。 |
Sargent: 2004年にACCENT共同研究として、私は3年DFSが5年OSの代替エンドポイントとなることを報告しました。当時、結腸癌患者の約80%が最初の3年以内に再発することがわかっており、また、再発後の生存期間は約1年でした。
3年以内に患者の80%が再発し、彼らのほぼすべてが1年以内に死亡するのであれば、自然と3年DFSと5年OSは近似します。3年と5年の間は“2年”であり、患者はその半分に当たる1年間生存したからです。
現在も再発率は変わっていませんが、分子標的治療薬や新しい治療法の開発により、再発後の生存期間は約2年に延長しました。ごく単純に考えて、結腸癌患者の再発後の生存期間が2倍になったのですから、以前と同じ計算式を用いるのであれば、3年と5年の間である“2年”も2倍(4年)にする必要があるのではないか―― このようにして、我々は7年OSに注目したのです。
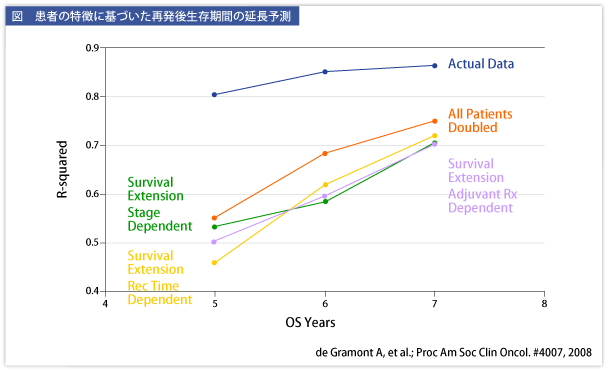
そして、我々は実際の患者データを使って検証を始めました。まず「再発した患者は2倍長く生きる」と仮定して、再発後の全患者の生存率を2倍にし、患者が再発した場合は必ず亡くなるまでデータを取りました。きわめて単純な仮説に基づいたデータセットですが、それほど非現実的なものではありませんでした。というのも、現実に再発後の生存期間が延長していたからです。
次に、昨年のASCOでのO'Connell先生の報告(#4009, 2007)に基づいて高度な分析を行いました。O'Connell先生の報告は、再発したstage IIおよびIII結腸癌患者の再発後生存期間を患者の特徴によって検証したもので、「time to recurrence(TTR)が短い患者は、TTRが長い患者に比べて再発後の生存期間が短縮される」「原発癌がstage IIの患者は原発癌がstage IIIの患者よりも再発後の生存期間が長い」ことなどを示しました。
我々は彼の発表内容に従って仮説を立て、可能な範囲で、個々の患者があとどれだけ生存できるのかを患者の特徴ごとに予測しようと試みました(図)。 |
 |
| 坂本: その公式はかつてないほど複雑なものなのでしょうが、より正確な結果を導き出すことが期待できそうですね。 |
| Sargent: ええ、そうなることを願っています。ただ、これまでの研究からわかったことですが、シンプルな方法で行うか複雑な方法で行うかは、さほど重要ではないのです。我々の研究で得られた生存曲線では、全症例において3年DFSと7年OSの相関が非常に強くなっています。OSで統計学的な有意差を得るためには、患者を6〜7年フォローアップする必要があると考えたほうがよいでしょうね。 |
| 坂本: MOSAIC試験やNSABP C-07試験などの新しい臨床試験についてはどのようにお考えですか。 |
Sargent: MOSAIC試験、NSABP C-07試験、PETACC-3試験、CALGB C89803試験、X-ACT試験―― これらの新しい臨床試験においては、3年DFSが7年OSを予知する指標になると考えています。すでに上記5試験の全データを保有していますので、そのデータをもとに検証を行い、我々の考えている新しいモデル「3年DFSは7年OSと相関する」を立証したいと考えています。
新しい臨床試験が実施されると、当然ながらOSも変わっていきます。ですから、我々は絶えず自分たちのモデルを検討し、修正・変更を加え、新たなデータに基づいてそれを立証するようにしています。また、新しいモデルを開発する際には、独立したデータによって検証する必要があります。とある患者でモデルを開発し、同一患者で検証したとしても、それには確たる根拠があるとはいえません。モデルを開発し、その開発の際に使用したデータから完全に独立したデータセットで、改めて検証する必要があるのです。 |
| 坂本: OSに替えて用いることができるsurrogate endpointの正確な評価は、臨床試験の根幹にかかわる大切な問題の1つと考えております。新しい臨床試験データでの研究成果のご発表を心待ちにしています。本日はお忙しいところ、どうもありがとうございました。 |
| Sargent: こちらこそ。私もお話しできて嬉しかったです。 |
 |





