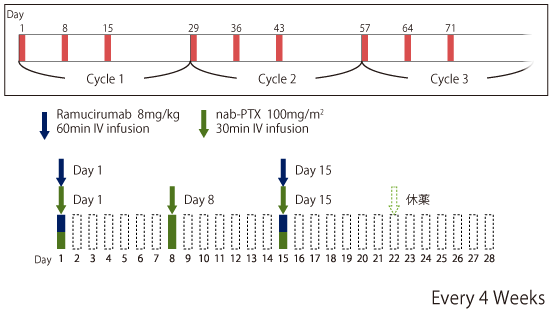
Weekly nab-Paclitaxel(nab-PTX)+Ramucirumab
 |
Bando H, et al.: Eur J Cancer. 91: 86-91, 2018 |
ナノ粒子アルブミン結合Paclitaxel(nab-Paclitaxel)は従来のPaclitaxel(PTX)と比較して過敏性反応のリスクが少なく、アルコール不耐患者にも投与可能、という利便性を有している。ABSOLUTE試験1)では、主要評価項目である全生存期間(OS)においてnab-PTX毎週投与法は従来のPTX毎週投与法に対する非劣性を示した。そこで、二次治療の標準治療であるweekly PTX+Ramucirumab(RAM)療法のPTXをnab-PTXに置き換えたweekly nab-PTX+RAM療法の有効性と安全性を検討する試験が計画された。
◆nab-PTX+RAM療法の第II相試験2)
本試験は、初回化学療法であるフッ化ピリミジン系薬剤を含む治療に不応となった切除不能進行・再発胃癌患者の2次化学療法として、nab-PTX+RAM療法の有効性と安全性を検証する国内多施設共同第II相試験である。45症例が登録され、43症例がnab-PTX+RAM療法を実施された。
■有効性
投与期間中央値は5.6ヵ月(範囲0.5-10.2ヵ月)、治療サイクル中央値は6サイクル(範囲1-11サイクル)であった。主要評価項目である奏効割合(ORR)は54.8%(90% CI: 41.0-68.0)であり、ORRの信頼区間の下限は閾値奏効割合の20%を上回り、有望な結果と報告された。また、病勢制御割合(DCR)は92.9%(95% CI: 80.5-98.5)、無増悪生存期間(PFS)中央値は7.6ヵ月(95% CI: 5.4-8.1)、OSの中央値は未到達であった。前治療にプラチナ製剤が入っていない症例が30%含まれたり、測定可能病変がある症例のみだったりと、若干背景が異なるが、RAINBOW試験の日本人サブグループ3)においてweekly PTX+RAM療法のORR 41%、DCR 94%、PFS中央値5.6ヵ月であることを考えると、有望な結果であった。
| nab-PTX+RAM群(n=43) | |
| ORR | 54.8% |
| DCR | 92.9% |
| PFS中央値 | 7.6ヵ月 |
| OS中央値 | 未到達 |
■安全性
Grade 3以上の有害事象は、88.4%に認められた。その中でも好中球減少症76.7%、白血球減少症27.9%と、発現割合が高く認められた。発熱性好中球減少症は4.7%であった。
RAINBOW試験の日本人サブグループにおいてweekly PTX+RAM療法でのGrade 3以上の好中球減少症は66.2%であり、nab-PTX+RAMでは、PTX投与量が90mg/m2に増量されることもあり、多く認められた。発熱性好中球減少症は4.4%であったが、これは選ばれた患者に対して、限られた施設で行われた第II相試験と、より一般臨床に近い患者が登録された第III相試験の違いである。日常診療では、より発熱性好中球減少症に注意すべきと考えられる。
レジメン解説執筆:国立がん研究センター中央病院 消化管内科 今関 洋 先生
References
GI cancer-net
消化器癌治療の広場
