IFL亄Bevacizumab椕朄偺桪墇惈傪徹柧偟偨AVF2107g帋尡
丂VEGF偼撪旂嵶朎偺憹怋傪挷愡偡傞場巕偱偁傝丄偝傑偞傑側VEGF庴梕懱偵寢崌偡傞儕僈儞僪偱偡丅偙偺宱楬偱嵟弶偵奐敪偝傟偨暘巕昗揑栻偼Bevacizumab偱偡偑丄尰嵼偼VEGF trap偱偁傞Aflibercept偺傎偐丄悢乆偺栻嵻偑奐敪偝傟偰偄傑偡丅VEGF偼戝挵娻偺恑峴憗婜偵敪尰偟丄梊屻晄椙偲娭學偟偰偄傑偡丅偟偐偟丄VEGF慾奞栻偵傛偭偰儀僱僼傿僢僩偑摼傜傟傞姵幰傪梊應偡傞儅乕僇乕偼尒偮偐偭偰偍傜偢丄庮釃弅彫岠壥傕尷傜傟偰偄傑偡丅
丂Bevacizumab偺桳岠惈偑妋擣偝傟偨嵟弶偺帋尡偼丄愗彍晄擻戝挵娻枹帯椕椺偵懳偡傞柍嶌堊壔戞II憡帋尡偱丄OS (overall survival) 拞墰抣偼bolus 5-FU/LV孮偺13.8儠寧偵懳偟丄Bevacizumab 5mg/kg暪梡孮偱偼21.5儠寧丄10mg/kg暪梡孮偱偼16.1儠寧偲墑挿偟傑偟偨3)丅
丂堦曽丄IFL偲偺暪梡傪専摙偟偨AVF2107g帋尡偱偼丄OS拞墰抣偑IFL 孮偺15.6儠寧偵懳偟IFL亄Bevacizumab孮偱偼20.3儠寧 (HR=0.66, p< 0.001)丄PFS (progression-free survival) 拞墰抣偼偦傟偧傟6.2儠寧丄10.6儠寧 (HR=0.54, p< 0.001)丄憈岠棪偼偦傟偧傟34.8亾丄44.8亾 (p=0.004) 偱偁傝丄Bevacizumab暪梡偵傛偭偰桳堄偵夵慞偟傑偟偨4)丅撆惈偵偮偄偰偼丄IFL亄Bevacizumab孮偱偼grade 3/4偺桳奞帠徾偑桳堄偵懡偔丄摿偵崅寣埑偑懡偔傒傜傟偨傕偺偺丄埆怱丒歲揻丄壓棢丄崪悜梷惂丄寣愷徢側偳偺敪尰昿搙偵桳堄嵎偼側偔丄娗棟壜擻偱偟偨丅偙偺寢壥傪庴偗偰丄FDA偼Bevacizumab傪恦懍彸擣偟傑偟偨丅
FOLFOX亄Bevacizumab椕朄偺棤晅偗偲側偭偨NO16966帋尡
丂NO16966帋尡偼丄1st-line偲偟偰偺XELOX偍傛傃FOLFOX4偺桳梡惈偲Bevacizumab偺忋忔偣岠壥傪斾妑偟偨丄2亊2僨僓僀儞偺柍嶌堊壔斾妑帋尡偱偡丅杮帋尡偱偼XELOX/FOLFOX4孮偲斾傋丄XELOX/FOLFOX4亄Bevacizumab孮偱PFS偺桳堄側墑挿偑帵偝傟傑偟偨 (8.0儠寧 vs. 9.4儠寧, HR=0.83, p=0.0023)5)丅偟偐偟丄偦偺嵎偼1.4儠寧偵夁偓偢丄IFL偲偺暪梡帪偵擣傔傜傟偨4.4儠寧偺嵎偵斾傋傞偲彫偝側傕偺偱偟偨丅
丂偦偺堦場偲偟偰丄杮帋尡偱偼Oxaliplatin (L-OHP) 偵傛傞枛徑恄宱忈奞偺偨傔偵丄戝敿偺姵幰偑PD偵払偡傞慜偵帯椕傪拞巭偟偨偙偲偑巜揈偝傟偰偄傑偡丅OS拞墰抣傕XELOX/FOLFOX4孮偑19.9儠寧偱偁傞偺偵懳偟丄XELOX/FOLFOX4亄Bevacizumab暪梡孮偱偼21.3儠寧偱偁傝丄Bevacizumab暪梡偵傛傞桳堄側墑挿偼帵偝傟傑偣傫偱偟偨丅
丂偙偺傎偐丄柍嶌堊壔斾妑帋尡偱偼偁傝傑偣傫偑丄堦師帯椕偲偟偰偺Bevacizumab偺暪梡岠壥傪専摙偟偨偺偑BICC-C 帋尡偱偡6)丅杮帋尡偺OS拞墰抣偼FOLFIRI孮23.1儠寧偵懳偟FOLFIRI亄Bevacizumab 孮偱偼28.0儠寧丄mIFL孮17.6儠寧偵懳偟丄mIFL亄Bevacizumab 孮偱偼19.2儠寧偱偟偨丅
Medicare僨乕僞偐傜丄幚椪彴偵偍偗傞Bevacizumab偺忋忔偣岠壥傪専徹
丂偙偙偱変乆偺尋媶傪徯夘偟偨偄偲巚偄傑偡丅変乆偼暷崙棫娻尋媶強 (NCI) 偵傛傞摑寁僨乕僞儀乕僗乬SEER乭偵搊榐偝傟偨Medicare偺棙梡姵幰傪懳徾偵丄1st-line偵偍偗傞Bevacizumab暪梡偺桳岠惈乗乗乬effectiveness乭傪専摙偟傑偟偨7)丅偛懚抦偐偲巚偄傑偡偑丄Medicare偼傾儊儕僇偺崅楊幰岦偗岞揑堛椕曐尟偱偡丅
丂乬Efficacy乭偲乬effectiveness乭偼堦尒摨偠偵巚偊傞偐傕偟傟傑偣傫偑丄efficacy偑乬斾妑懳徠帋尡乭偵偍偗傞栻嵻偺岠壥傪堄枴偡傞偺偵懳偟丄effectiveness偼乬幚椪彴乭偱偺栻嵻偺岠壥傪堄枴偟傑偡丅幚椪彴偱偼丄椪彴帋尡偱偼晄揔奿偵側傞傛偆側姵幰傕娷傑傟傑偡偟丄搳梌偺抶墑傗尭検側偳傕堦掕偟偰偄傑偣傫丅壔妛椕朄傪愭峴偟丄屻偐傜Bevacizumab傪奐巒偡傞応崌傕偁傝傑偡丅
丂変乆偼Medicare僨乕僞偐傜丄2002擭偐傜2007擭偵偐偗偰戝挵娻偲恌抐偝傟偨65嵨埲忋偺姵幰104,524椺傪拪弌偟丄偝傜偵乽stage IV乿乽恌抐偐傜6儠寧埲撪偵壔妛椕朄傪巤峴乿乽5-FU/Capecitabine傪巊梡乿乽僼僢壔僺儕儈僕儞宯栻嵻偺弶夞搳梌偐傜30擔埲撪偵L-OHP傑偨偼CPT-11傪暪梡乿側偳偺忦審傪枮偨偟偨2,526椺傪懳徾偵夝愅傪峴偄傑偟偨丅
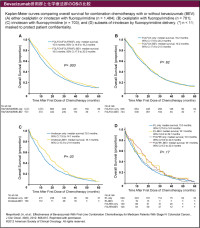
丂偦偺寢壥丄壔妛椕朄 (FOLFOX / FOLFIRI / IFL) 孮 偺OS拞墰抣偼15.9儠寧偱偁偭偨偺偵懳偟丄Bevacizumab暪梡壔妛椕朄孮偱偼19.0儠寧偱偁傝丄桳堄側墑挿偑擣傔傜傟傑偟偨 (p=0.003) 乵恾2-A乶丅堦曽丄壔妛椕朄偺儗僕儊儞暿偱偼丄FOLFOX孮偲FOLFOX亄Bevacizumab孮偺OS拞墰抣偼偳偪傜傕19.2儠寧偱嵎偼傒傜傟傑偣傫偱偟偨偑丄FOLFIRI/IFL孮偱偼13.0儠寧丄FOLFIRI/IFL亄Bevacizumab孮偱偼18.1儠寧偲桳堄側墑挿偑擣傔傜傟傑偟偨 (p=0.03) 乵恾2-B, C乶丅
丂偙偙偱丄乽傎偐偺暪梡壔妛椕朄傛傝傕岠壥偺楎傞IFL偩偐傜偙偦丄Bevacizumab暪梡偺傋僱僼傿僢僩偑摼傜傟偨偺偱偼丠乿偲偄偆媈栤偑惗偠傑偡丅変乆傕FOLFIRI偲IFL傪暿乆偵専摙偟偨偐偭偨偺偱偡偑丄Medicare偺惪媮僨乕僞偐傜IFL偲FOLFIRI傪惓妋偵嬫暿偡傞偺偼崲擄偱偡丅偦偙偱姰帏側掕媊偲偼偄偊傑偣傫偑丄曋媂揑偵乽8廡娫偵CPT-11傪5夞埲忋搳梌偟偨応崌傪IFL乿乽4夞埲撪偺応崌傪FOLFIRI乿偲傒側偟偰斾妑傪峴偄傑偟偨丅偦偺寢壥丄OS拞墰抣偼IFL孮偱13.0儠寧丄FOLFIRI孮偱偼13.3儠寧偲傎偲傫偳嵎偼側偔丄偄偢傟傕Bevacizumab偺暪梡偵傛傝18.1儠寧偵墑挿偟傑偟偨乵恾2-D乶丅
丂偙偺傛偆偵丄変乆偺専摙偱偼CPT-11儀乕僗偺壔妛椕朄偱偼懡彮偺Bevacizumab暪梡偺岠壥偑傒傜傟偨傕偺偺丄L-OHP儀乕僗偺壔妛椕朄偱偼擣傔傜傟側偄偲偄偆寢壥偵側傝傑偟偨丅
杮暥偼偙偙傑偱偱偡丅
仯 偙偺儁乕僕偺僩僢僾傊