背景と目的
局所進行直腸癌に対しては、5-FUを用いた周術期治療により局所再発率は6%未満となったものの、25%に遠隔転移がみられるため生存率は65%と低いままである。Stage III結腸癌術後においてFOLFOX、XELOXは5-FUと比較し生存を改善することが知られているが、直腸癌にそのまま応用するためには前向きの試験が必要である。
PETACC 6試験は、同時期に始まったほかの4つの試験 (NSABP R04試験、ACCORD/PRODIGE 02試験、STAR試験、CAO/ARO/AIO-04試験) と同様に、局所進行直腸癌の周術期の5-FUにL-OHPの上乗せ効果を検証するために行われた。術前化学放射線療法の部分は、AIO/ARO試験の結果において高い忍容性と良好な抗腫瘍効果を得たことからCapecitabine ± L-OHPが選ばれ、同様に、術後補助化学療法の部分にはX-ACT試験、XELOXA試験で良好な結果が得られたCapecitabine vs. XELOXが選ばれた1-5)。
対象と方法
対象は、病理学的に腺癌と診断された直腸癌患者で、肛門縁より12cm以内、T3/4 and / or N+ (ステージングはMRI、またはEUS + CTによる)、切除可能もしくは術前化学放射線療法によりR0/1切除が期待される、WHO/ECOG PS 0-2の症例であった。
術前化学放射線療法は、Cape群、Cape + L-OHP群の両群で放射線治療50.4GyとCapecitabine (825mg/m2, 1日2回, 週末を除くday1-33) が投与され、さらにCape + L-OHP群では、L-OHP (50mg/m2, day1, 8, 15, 22, 29) が投与された (図1)。
術後補助化学療法は、両群でCapecitabine (1,000mg/m2, 1日2回, day1-14, 3週毎) が、さらにCape + L-OHP群では、L-OHP (130mg/m2, day1, 3週毎) がともに6サイクル投与された。
図1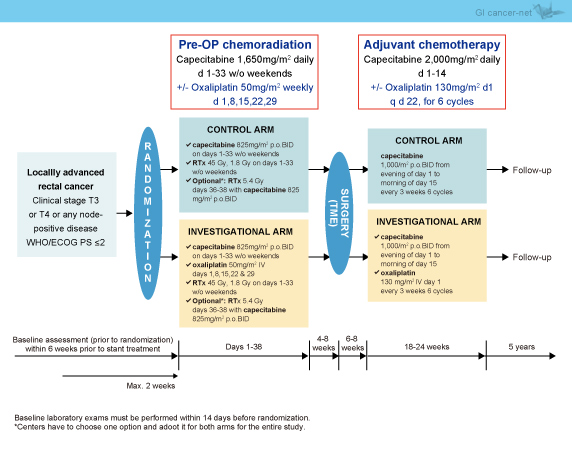
主要評価項目はDFS (disease-free survival) で、3年DFSを65%から72%に改善 (HR=0.763) するという仮説のもと、検出力80%、両側α=0.05で、必要症例数は1,090例であった。また、225イベントが起こった時点で中間解析を行うことが予定された。
副次評価項目はOS、局所再発、全身転移、病理学的ダウンステージ、病理学的CR (ypT0N0)、腫瘍縮小、肛門括約筋温存率であった。
結果
2008年11月~2011年9月に1,094例が登録され、Cape群、Cape + L-OHP群に547例ずつ無作為に割り付けられた。予定どおり術前化学放射線療法が行われた症例はCape群100%、Cape + L-OHP群98%であり、手術が行われた症例はそれぞれ98%、97%であった。
術後補助化学療法が開始された症例は、CAO/ARO/AIO-04試験 (#3500) より低く、Cape群79%、Cape + L-OHP群73%であったが、Cape + L-OHP群の9%で術前の有害事象などによりL-OHPの投与が行われなかったため、実際に術後にCape + L-OHPの投与が行われたのは63%であった (図2)。
図2
患者背景は、年齢、男女比、PS、stageは両群で差を認めなかった。なお、両群ともにstage IIが約20%、stage IIIが約70%と、stage III症例が多かった。
術前化学放射線療法の毒性とコンプライアンスを表1に示す。Cape + L-OHP群ではCape群の2倍以上のgrade 3/4の毒性を認め、多くは消化器毒性であり、両群で各1例に治療関連死も認めた。コンプライアンスの検討では、放射線治療はCape群99%、Cape + L-OHP群96%、Capecitabineはそれぞれ95%、84%であり、Cape + L-OHP群でL-OHPを80%超投与された症例は81%であった。
表1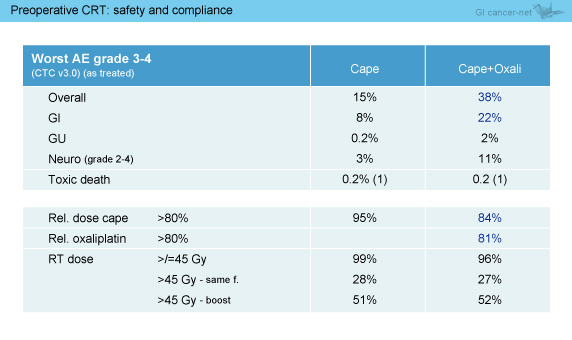
手術に関する検討では、8週超の治療遅延はCape群12%、Cape + L-OHP群16%に認め、TMEは両群とも89%で行われた。なお、手術合併症の比率 (42% vs. 46%)、治療関連死 (0.9% vs. 0.6%) は両群で差を認めなかった。
Cape群97%、Cape + L-OHP群96%でR0切除が行われ、R2切除となったのはCape群0.2%、Cape + L-OHP群0.4%であり、肛門括約筋は両群ともに72%で温存された (表2)。病理学的CRはCape群12%、Cape + L-OHP群14%で、有意差は認めないもののCape + L-OHP群で良好な傾向であった。
表2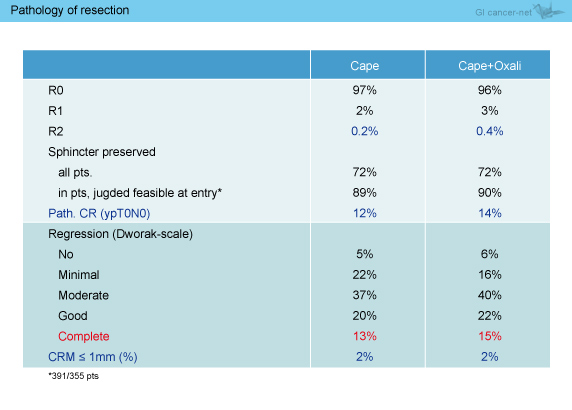
術後補助化学療法はCape群80%、Cape + L-OHP群75%で開始され、Cape + L-OHP群で実際にL-OHPを投与したのは65%であった。予定された6サイクルを完了できたのはCape群69%、Cape + L-OHP群57%であり、投与量、症例は大幅に減少した。なお、術後補助化学療法が行われなかった理由は、術前治療の毒性が最も多かった。
主要評価項目であるDFSの検討では、Cape群、Cape + L-OHP群において、R2切除率 (1例 vs. 4例)、局所再発 (17例 vs. 9例)、遠隔転移 (89例 vs. 81例)、および腫瘍増悪・再発全体 (107例 vs. 94例) において有意な差を認めなかった。
観察期間中央値31ヵ月時点での3年DFSはCape群74.5%、Cape + L-OHP群73.9%であり、両群に有意差を認めなかった (HR=1.04, 95% CI: 0.81-1.33, p=0.78) (図3)。また、割り当てられた術後補助化学療法が開始された症例だけに絞ってDFSの検討を行ったが、HR=0.92 (p=0.63) であり、観察時点で有意差を認めなかった。
図3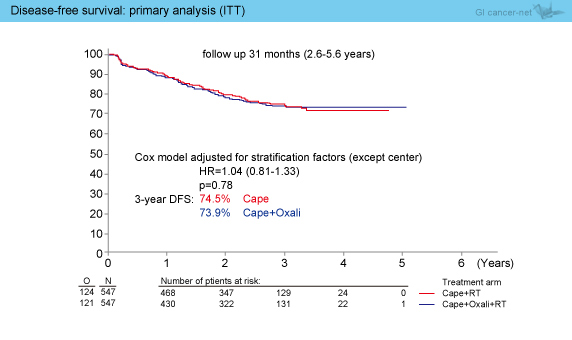
3年時点での局所再発率はCape群7.6%、Cape + L-OHP群4.6% (p=0.094)、遠隔転移率はそれぞれ19.2%、17.6%であり (p=0.542)、いずれも有意差を認めなかった (図4)。また、臨床病理学的検討でも、年齢、性別、PS、T stage、N stageのいずれにおいても両群に差を認めなかった。
図4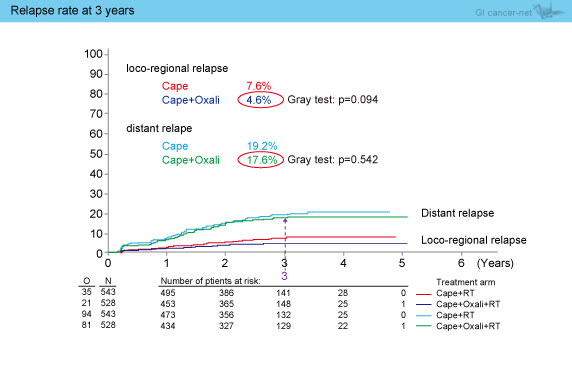
3年OSは、Cape群89.5%、Cape + L-OHP群87.4%であり、両群に差を認めなかった (HR=1.31, 95% CI: 0.89-1.93, p=0.179) (図5)。
図5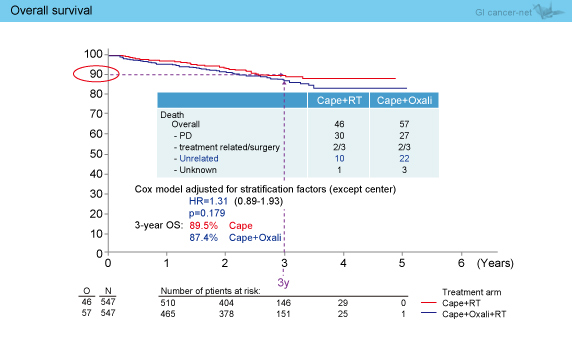
結論
局所進行直腸癌に対するCapecitabineによる周術期化学放射線療法において、L-OHPの併用は毒性によりコンプライアンスを低下させたが、R0切除率、病理学的CR率、肛門括約筋温存率を改善しなかった。また、観察期間中央値2.6年時点での中間解析では、術前術後にL-OHPを併用することによるDFS改善は認めなかった。
なお、両群において局所の抗腫瘍効果、R0/1切除率、局所再発もしくは遠隔転移において期待されたより良好な結果であった。今後追跡を行うことによりHRの期待値0.763を下回る確率は7%しかないが、可能性は残されており、最終解析には最低2年の経過観察が必要である。
コメント
直腸癌の術前 (化学) 放射線療法については多くの臨床試験が行われている。その結果をみると、術前 (化学) 放射線療法には局所再発の抑制効果は認められるものの、いわゆるSwedish rectal cancer trial以外では全生存期間の延長効果はみられていない (座談会参照)。今年の米国臨床腫瘍学会年次集会では、直腸癌に対する術前化学放射線療法と術後補助化学療法の効果を検討した研究結果の報告が4題あった (下表)。
本研究では、Cape群とCape + L-OHP群で術前化学放射線療法と術後補助化学療法に用いるCapecitabineの量が揃えられた。したがって、純粋にL-OHPの上乗せ効果を検証した研究であると言える。その結果、L-OHPには3年DFSと3年OSについて上乗せ効果は認められなかった。一方、L-OHPの併用で3年DFSの改善がみられた#3500では、術後補助化学療法に強力なレジメンが用いられており、純粋なL-OHPの上乗せ効果を検討した研究とは言えない。これらの結果から、有害事象の増加等も勘案し、直腸癌に対する術前化学放射線療法にL-OHPを用いることを推奨するエビデンスはないと考えられる。
| 演題 | 標準治療 | 試験治療 | setting | 症例数 | 期待値 (3年DFS) |
結果 (3年DFS) |
||||
|---|---|---|---|---|---|---|---|---|---|---|
| 標準治療 | 試験治療 | 標準治療 | 試験治療 | HR | p値 | |||||
| #3603 | Capecitabine or 5-FU + RT | L-OHP併用 | 術前 | 1,284 | 64.2% (5年DFS) |
69.2% (5年DFS) |
0.34 | |||
| #3500 | 5-FU + RT | L-OHP併用 | 術前後 | 1,236 | 75% | 82% | 71.2% | 75.9% | 0.79 | 0.03 |
| #3501 | Capecitabine + RT | L-OHP併用 | 術前後 | 898 | 65% | 72% | 74.5% | 73.9% | 1.04 | 0.78 |
| #3502 | FL | L-OHP併用 | ypStage II/IIIの術後 | 321 | 70% | 78% | 62.9% | 71.6% | 0.63 | 0.032 |
(レポート:中村 将人 監修・コメント:大村 健二)
- Reference
-
- 1) Rodel C, et al.: J Clin Oncol. 21(16): 3098-3104, 2003[PubMed]
- 2) Rodel C, et al.: J Clin Oncol. 25(1): 110-117, 2007[PubMed]
- 3) Twelves C, et al.: N Engl J Med. 352(26): 2696-2704, 2005[PubMed]
- 4) Schmoll HJ, et al.: J Clin Oncol. 25(1): 102-109, 2007[PubMed]
- 5) Haller DG, et al.: J Clin Oncol. 29(11): 1465-1471, 2011[PubMed]


