| |
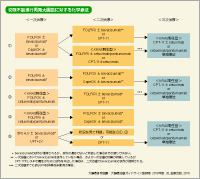
大村:NCCNの切除不能大腸癌に対する化学療法のアルゴリズムをみると、1st-lineにはBevacizumab + 化学療法の各レジメンが記載されています。しかし、Bevacizumabは2nd-line以降には登場せず、後の解説に「1st-lineでBevacizumabを使用しなかった場合、2nd-lineでの投与を考慮するのは妥当である」と記載されています6)。一方、わが国の大腸癌治療ガイドラインでは、2nd-lineにもBevacizumabの記載があります5 ) (図5)。この両者の違いは実臨床で混乱を招く可能性もあると思うのですが、先生方はどのようにお考えでしょうか。
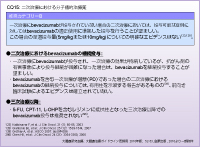
松本:日本の大腸癌治療ガイドラインでは、“Clinical Question”において、2nd-lineでのBevacizumab投与が推奨されるのは「1st-lineでL-OHPまたはCPT-11の有害事象のために治療を中止した場合」であり、「BBPのエビデンスは確立されていない」と明記されています (表2)。NCCNと同じく、決してBBPを推奨しているわけではありません。
佐藤:今回のガイドライン改訂で初めてBevacizumab、Cetuximab、Panitumumabの3つの分子標的治療薬が出揃いましたが、実臨床では1st-lineでBevacizumabを使った後はどうするのか、困惑している人も多いのではないかと思います。BRiTEは観察研究であり、RCTのように症例選択をしていないからこそ、逆に実臨床に近いとProf. Grotheyもおっしゃっています。このアルゴリズム (図5) とClinical Question (表2) を見る限り、BBPを推奨とまではいかなくとも、主治医の選択肢のひとつとして選ぶことは許容されると考えます。

瀧井:日本のガイドラインでは、例えば「FOLFOX±Bevacizumab」というように、Bevacizumabの併用についてはすべて“±”で示されています (図5)。これは、「1st-lineでBevacizumabを使用しなかった症例には2nd-lineでBevacizumabを使用する」という意味にもとれますし、「1st-line、2nd-lineの両方でBevacizumabを使用してもよい」という意味にもとれますが、原則としては前者の捉え方になると思います。
また、BRiTEは実臨床に近いとおっしゃいましたが、Physicians’ choiceは多変量解析では出てこない多様な要素が含まれており、非常に偏ったデータを出すことも可能です。RCTを行わない限り、BBPを推奨することはできないと思います。
大村:確かに日本のガイドラインは、一見すると2nd-lineでBevacizumabの使用が推奨されているように思えますが、実はこれはPDではない。注釈を見ると、「1st-lineでCPT-11やL-OHPの毒性のために投与を中止した場合」であり、BBPを示したものではないのですね。
瀧井:「日本のガイドラインは2nd-lineでのBevacizumabの使用を認めている」という声も聞きますが、BBP自体は認めていないのです。
 |