戨撪丗 懕偄偰丄2nd-line偵偍偗傞aggressive approach偲峈EGFR峈懱栻偺埵抲偯偗偵僥乕儅傪堏偟偨偄偲巚偄傑偡丅傑偢偼擔杮偺尰忬偵偮偄偰丄媑栰愭惗偵儗僋僠儍乕傪偍婅偄偟傑偡丅

擔杮偵偍偗傞愗彍晄擻恑峴丒嵞敪戝挵娻偺2nd-line帯椕偺尰忬
媑栰 岶擵愭惗

媑栰丗 摉堾偵偍偗傞愗彍晄擻恑峴丒嵞敪戝挵娻帯椕偺尰忬偵偮偄偰丄2nd-line傪拞怱偵偍榖偟傑偡丅擔杮偱愗彍晄擻恑峴丒嵞敪戝挵娻偵巊梡壜擻側暘巕昗揑帯椕栻偼峈VEGF峈懱栻 (Bevacizumab) 偲峈EGFR峈懱栻 (Cetuximab丄Panitumumab) 偺2庬椶偱偡丅偄偢傟偺栻嵻傕暷崙偐傜3乣4擭抶傟偱彸擣偝傟傑偟偨丅偙偺偆偪摉堾偱嵟傕傛偔巊傢傟偰偄傞偺偼Bevacizumab偱丄峈EGFR峈懱栻偱偼Panitumumab偑懡偔巊傢傟偰偄傑偡丅
丂擔杮偺戝挵娻帯椕僈僀僪儔僀儞偵偍偗傞愗彍晄擻戝挵娻偵懳偡傞帯椕愴棯偼丄NCCN僈僀僪儔僀儞偲傎傏摨偠偱偡丅擔杮偼庮釃撪壢堛偺悢偑彮側偄偨傔丄戝敿偼奜壢堛偑壔妛椕朄傪峴偭偰偄傑偡丅
丂尰嵼丄擔杮偵偍偄偰1st-line偱嵟傕懡偔梡偄傜傟傞儗僕儊儞偼FOLFOX / XELOX + Bevacizumab偲悇應偝傟傑偡丅2nd-line偵偍偄偰偼丄Bevacizumab傪娷傓儗僕儊儞傗峈EGFR峈懱栻傪娷傓儗僕儊儞偑幚巤偝傟偰偄傞傛偆偱偡丅1st-line帯椕偱PD偑擣傔傜傟偨屻傕Bevacizumab傪巊偄懕偗傞愴棯 (Bevacizumab beyond progression: BBP)25) 傪偲偭偰偄傞堛巘傕彮側偔偁傝傑偣傫丅3rd-line偼峈EGFR峈懱栻偑拞怱偱丄CPT-11傗FOLFIRI偲偺暪梡偺傎偐丄扨嵻偱傕巊傢傟偰偄傞傛偆偱偡丅
丂擔杮偱偼KRAS 堚揱巕栰惗宆偱偁偭偰傕丄Bevacizumab偑1st-line偵嵟揔側暘巕昗揑帯椕栻偲峫偊傜傟偰偄傑偡丅偦傟偼丄1st-line偱偺桳岠惈偵偍偄偰Bevacizumab傪忋夞傞峈EGFR峈懱栻偺僄價僨儞僗偑側偄偨傔偱偡丅
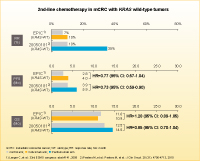
丂巹帺恎偼Panitumumab偑KRAS 堚揱巕栰惗宆姵幰偺2nd-line偵嵟揔側暘巕昗揑帯椕栻偱偁傞偲峫偊偰偄傑偡丅偦偺棟桼偼丄2nd-line偲偟偰偺FOLFIRI 亇 Panitumumab 傪専摙偟偨20050181帋尡26) 偲丄CPT-11 亇 Cetuximab傪専摙偟偨EPIC帋尡27) 偱偺KRAS 堚揱巕栰惗宆姵幰偺惉愌傪斾妑偡傞偲丄憈岠棪傕OS傕Panitumumab暪梡偺傎偆偑椙岲偱偁傞偨傔偱偡 (恾11)丅
偙傟傜2偮偺帋尡偵偼偄偔偮偐偺尷奅偑偁傝傑偡偑丄20050181帋尡偼慜岦偒偵KRAS 堚揱巕専嵏傪峴偭偰2nd-line偲偟偰偺Panitumumab偺椪彴揑堄媊傪昡壙偟偰偄傞偙偲偐傜丄僨乕僞偺幙偲偄偆柺偱偺怣棅惈偼崅偄偲峫偊傜傟傑偡丅
丂偙偆偟偨偙偲偐傜丄摉堾偱偼1st-line偱FOLFOX / XELOX + Bevacizumab傪峴偭偨KRAS 堚揱巕栰惗宆姵幰偵懳偟偰偼丄2nd-line偲偟偰FOLFIRI / CPT-11 + Panitumumab傪姪傔偰偄傑偡丅
丂Cetuximab偲Panitumumab偺憡堘揰偲椶帡揰傪梫栺偡傞偲丄搳梌僗働僕儏乕儖偼Cetuximab偑枅廡搳梌偱偁傞偺偵懳偟丄Panitumumab偼2廡枅搳梌偱偁傞揰偑堎側傝傑偡丅暃嶌梡偵娭偟偰偼丄Panitumumab偺曽偑旂晢撆惈偑傗傗嫮偄報徾偑偁傝傑偡偑丄infusion reaction偼彮側偄偙偲偑嫇偘傜傟傑偡 (昞3)丅