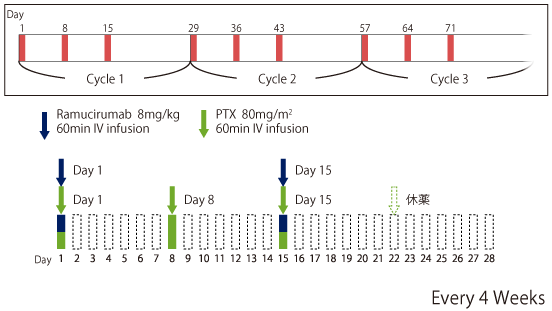
Weekly Paclitaxel(PTX)+Ramucirumab
 |
Wilke H, et al.: Lancet Oncol. 15(11): 1224-1235, 2014 |
Ramucirumabは、血管内皮増殖因子受容体-2(VEGFR-2)に対する完全ヒト型IgG1モノクローナル抗体であり、VEGF-A、VEGF-C、VEGF-DのVEGFR-2への結合を阻害することにより、VEGFR-2の活性化を阻害し、内皮細胞の増殖・遊走・生存を阻害し、腫瘍血管新生を阻害すると考えられている。日本においては2015年3月に「治癒切除不能な進行・再発の胃癌」に対して承認を取得し、その他、結腸・直腸癌、非小細胞肺癌や肝細胞癌に対する有用性が確認され、適応追加の承認を受けている。
◆RAINBOW試験1)
RAINBOW試験は、1st-lineとしてフッ化ピリミジン系製剤とプラチナ系製剤を投与された進行胃腺癌または食道胃接合部腺癌の2nd-lineとして、Paclitaxel(PTX)に対するRamucirumab(RAM)の上乗せ効果を検証する国際多施設共同第III相試験である。適格症例665例がPTX+RAM群とPTX+プラセボ群に1:1の割合で無作為化された。
■有効性
主要評価項目である全生存期間(OS)中央値は、PTX+プラセボ群7.4ヵ月、PTX+RAM群9.6ヵ月であり、RAM併用により有意な延長を認めた(HR=0.807、95% CI: 0.678-0.962、p=0.0169)。また、副次評価項目である無増悪生存期間(PFS)中央値においても、PTX+プラセボ群2.9ヵ月、PTX+RAM群4.4ヵ月であり、RAM併用により有意な延長を認めた(HR=0.635、95% CI: 0.536-0.752、p<0.0001)。
一方、日本人サブグループ(n=140)の解析2)では、OS中央値は、PTX+プラセボ群11.5ヵ月、PTX+RAM群11.4ヵ月であり、両者に有意な差は認めなかった(HR=0.88、95% CI: 0.60-1.28、p=0.511)が、PFSは中央値でPTX+プラセボ群2.8ヵ月、PTX+RAM群5.6ヵ月と有意な延長を示し(HR=0.50、95% CI: 0.35-0.73、p=0.0002)、奏効割合でもPTX+プラセボ群19.4%、PTX+RAM群41.2%と有意差を示した(p=0.0035)。
| PTX+RAM群 (n=330) |
PTX+プラセボ群 (n=335) |
HR (95% CI) |
P値 | |
| OS中央値 | 9.6ヵ月 | 7.4ヵ月 | 0.807 (0.678-0.962) |
0.0169 |
| PFS中央値 | 4.4ヵ月 | 2.9ヵ月 | 0.635 (0.536-0.752) |
<0.0001 |
■安全性
Grade 3以上の有害事象はPTX+RAM群/PTX+プラセボ群において、82%/63%に認められた。PTX+RAM群において好中球減少症(41%/19%)、白血球減少症(17%/7%)、疲労(12%/5%)、腹痛(6%/3%)、高血圧症(14%/2%)等の発現割合が高く認められた。一方で、発熱性好中球減少症(3%/2%)は発現割合に差はなかった。
サブグループ解析2)では、日本人サブグループ、欧米人サブグループとも、Grade 3以上の出血、消化管穿孔がPTX+RAM群に多く認められた。
日本人サブグループでは欧米人と比較して、Grade 3以上の好中球減少症が多く認められた。
レジメン解説執筆:国立がん研究センター中央病院 消化管内科 今関 洋 先生
References
- 副作用対策講座「高血圧」
GI cancer-net
消化器癌治療の広場
