IrinotecanپiCPT-11پj’Pچـ
 |
Bang YJ, et al.: Ann Oncol. 29(10): 2052-2060, 2018 |
CPT-11—أ–@‚حپA2ڈT‚²‚ئ‚ةCPT-11 150mg/m2‚ًگأ’چ‚·‚éژ،—أ–@‚إ‚ ‚éپBCPT-11‚حڈd“ؤ‚ب•›چى—pپi“ء‚ةچD’†‹…Œ¸ڈپj‚جƒٹƒXƒN—\‘ھ‚ج‚½‚ك‚جˆâ“`ژq‘½Œ^Œںچ¸‚ھ•غŒ¯گf—أ‚إ”F‚ك‚ç‚ê‚ؤ‚¢‚éپBCPT-11‚حSN-38‚ة‘مژس‚³‚ê‚ؤچRژîل‡Œّ‰ت‚ً”ٹِ‚·‚é‚ھپASN-38‚حUDP-ƒOƒ‹ƒNƒچƒ“ژ_“]ˆعچy‘fپiUGTپj‚جˆê‚آ‚إ‚ ‚éUGT1A1‚ة‚و‚ء‚ؤƒOƒ‹ƒNƒچƒ“ژ_•ّچ‡‚ًژَ‚¯‚ؤ•sٹˆ‰»‚³‚êپAژه‚ة’_ڈ`‚ض”rں•‚³‚ê‚éپBUGT1A1ˆâ“`ژq‚ج‘½Œ^‚ھ‚ ‚éڈا—ل‚إ‚حپASN-38‚ج‘مژس‚ھ’ل‰؛‚µپACPT-11‚ج—LٹQژ–ڈغ‚ھ‹‚”Œ»‚·‚éپBUGT1A1*6‚ئUGT1A1*28‚ج‚¢‚¸‚ê‚©‚ھƒzƒ‚گعچ‡Œ^پA‚à‚µ‚‚حƒ_ƒuƒ‹ƒwƒeƒچگعچ‡Œ^‚إ‚ ‚éڈêچ‡‚ح”¼—ت’ِ“x‚جŒ¸—ت‚ھŒں“¢‚³‚ê‚éپB
’°ٹا‚ج’ت‰كڈلٹQ‚ًچ‡•¹‚·‚éڈا—ل‚إ‚حپA’_ڈ`‚ة”rں•‚³‚ꂽSN-38‚ھچؤ‹zژûپi’°ٹجڈzٹآپj‚³‚êپAŒŒ’†”Z“x‚ھچ‚‚‚ب‚èڈd“ؤ‚ب—LٹQژ–ڈغ‚ًˆّ‚«‹N‚±‚·پB’°•آچا‚âچ‚“x• گ…ڈا—ل‚ة‘خ‚µ‚ؤ‚ح‹ضٹُ‚ئ‚ب‚ء‚ؤ‚¢‚éپB‚ـ‚½پA’_ڈ`”rں•Œ^‚ج–ٍچـ‚إ‚ ‚邱‚ئ‚©‚物لtڈا—ل‚ة‘خ‚µ‚ؤ‚à‹ضٹُ‚ئ‚ب‚ء‚ؤ‚¢‚éپB
پںJAVELIN Gastric 300ژژŒ±1)
JAVELIN Gastric 300ژژŒ±‚حپAگiچsˆفٹàپEگH“¹ˆفگعچ‡•”ٹàٹ³ژز‚ج3ژںژ،—أ‚ة‚¨‚¯‚éچRPD-L1چR‘جAvelumab‚ئˆمژt‘I‘ً‚ج‰»ٹw—أ–@پiCPT-11‚ـ‚½‚حweekly PaclitaxelپmwPTXپnپj‚ً”نٹr‚µ‚½‘½ژ{گف‹¤“¯چ‘چغ‘وIII‘ٹژژŒ±‚إ‚ ‚éپB
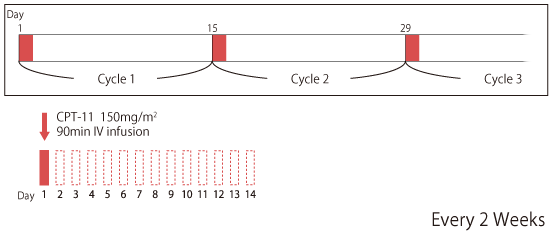
‰»ٹw—أ–@ŒQ‚إ‚حپACPT-11پi150mg/m2پAday 1,15پA4ڈT–ˆپj‚ـ‚½‚حwPTXپi80mg/m2پAday 1,8,15پA4ڈT–ˆپj‚ج‚ا‚؟‚ç‚©‚ھ”F‚ك‚ç‚ꂽ‚ھپA‰»ٹw—أ–@‚ج‘خڈغ‚ئ‚ب‚ç‚ب‚¢‚ئ”»’f‚³‚ꂽڈêچ‡‚حBSC‚à‹–—e‚³‚ꂽپB371گl‚ھ“oک^‚³‚êپAAvelumabŒQ‚ة185گlپA‰»ٹw—أ–@ŒQ‚ة186گl‚ھٹ„‚è•t‚¯‚ç‚ꂽپB‰»ٹw—أ–@ŒQ‚ج“à–َ‚حپA120گlپi64.5%پj‚ھCPT-11پA54گlپi29.0%پj‚ھwPTXپA3گlپi1.6%پj‚ھBSC‚إ‚ ‚ء‚½پi9گl‚حNo treatmentپjپB
پ،—LŒّگ«
JAVELIN Gastric 300ژژŒ±1)‚ة‚¨‚¯‚鉻ٹw—أ–@ŒQ‚جگ¬گر‚حپA‘tŒّٹ„چ‡پiORRپj4.3%پA–³‘ˆ«گ¶‘¶ٹْٹشپiPFSپj’†‰›’l2.7ƒ•ŒژپA‘Sگ¶‘¶ٹْٹشپiOSپj’†‰›’l5.0ƒ•Œژ‚إ‚ ‚ء‚½پBƒTƒuƒOƒ‹پ[ƒv‰ًگح‚إ‚حپACPT-11ŒQ‚جOS’†‰›’l5.4ƒ•ŒژپAwPTXŒQ‚جOS’†‰›’l4.7ƒ•ŒژپA‚ـ‚½پAAvelumabŒQ‚جگ¬گر‚حORR 2.2%پAPFS’†‰›’l1.4ƒ•ŒژپAOS’†‰›’l4.6ƒ•Œژ‚إ‚ ‚èپAAvelumabŒQ‚ح‰»ٹw—أ–@ŒQ‚ة‘خ‚µ‚ؤپAژه—v•]‰؟چ€–ع‚جOSپA•›ژں•]‰؟چ€–ع‚جPFSپAORRپA‚¢‚¸‚ê‚à—D‰zگ«‚ًژ¦‚¹‚ب‚©‚ء‚½پBˆب‰؛‚ةˆفٹà3ژںژ،—أ‚ئ‚µ‚ؤ‚جCPT-11—أ–@‚ج•ٌچگ‚ًژ¦‚·پB
| ژژŒ± | ژژŒ±ƒfƒUƒCƒ“ | ژ،—أƒ‰ƒCƒ“ | N | ƒŒƒWƒپƒ“ | ORR | PFS | OS |
| Bang YJ, et al.1) JAVELIN Gastric 300 |
Phase III | 3rd | 186 | پ– | 4.3% | 2.7ƒ•Œژ | 5.0ƒ•Œژ |
| 185 | Avelumab | 2.2% | 1.4ƒ•Œژ | 4.6ƒ•Œژ | |||
| Nishimura T, et al.2) | Retrospective | 3rd | 52 | CPT-11 | 3.0% | 2.3ƒ•Œژ | 4.0ƒ•Œژ |
| Makiyama A, et al.3) | Retrospective | 3rd/4th | 146 | CPT-11 | 6.8% | 3.2ƒ•Œژ | 6.6ƒ•Œژ |
| Kawakami T, et al.4) | Retrospective | 3rd | 50 | CPT-11 | 18.4% | 2.0ƒ•Œژ | 6.0ƒ•Œژ |
*CPT-11پinپپ120پjپAwPTXپinپپ54پjپABSCپinپپ3پjپANo treatmentپinپپ9پj
پ،ˆہ‘Sگ«
JAVELIN Gastric 300ژژŒ±1)‚ة‚¨‚¯‚éGrade 3ˆبڈم‚ج—LٹQژ–ڈغ‚حپA‰»ٹw—أ–@ŒQ‚إ31.6پ“پAAvelumabŒQ‚إ9.2پ“‚ة”F‚ك‚ç‚ꂽپB‰»ٹw—أ–@ŒQ‚إ‚جGrade 3ˆبڈم‚ج—LٹQژ–ڈغ‚حپAچD’†‹…Œ¸ڈ‚ھ13.0پ“‚إچإ‘½‚إ‚ ‚èپA”ٌŒŒ‰t“إگ«‚ح‚¢‚¸‚ê‚à4%–¢–‚إ‚ ‚ء‚½پB‚و‚è“ْڈيگf—أ‚ً”½‰f‚·‚é‚ئژv‚ي‚ê‚éپAŒم•ûژ‹“I‰ًگح2-4)‚©‚ç‚ج•ٌچگ‚إ‘½‚©‚ء‚½Grade 3ˆبڈم‚ج—LٹQژ–ڈغ‚حپAچD’†‹…Œ¸ڈپi19.2پ`24%پjپA•nŒŒپi19پ`30%پjپAگH—~•sگUپi5.5پ`14%پjپA””Mگ«چD’†‹…Œ¸ڈڈاپi6پ`12%پj‚ب‚ا‚إ‚ ‚ء‚½پB
ƒŒƒWƒپƒ“‰ًگàژ·•MپF“Œ‹ژœŒb‰ïˆم‰ب‘هٹw ڈء‰»ٹيپEٹج‘ں“à‰بپ@گ¼‘؛ ڈ® گوگ¶
References
- 1) Bang YJ, et al.: Ann Oncol. 29(10): 2052-2060, 2018 پmPubMedپnپmک_•¶ڈذ‰îپn
- 2) Nishimura T, et al.: Gastric Cancer. 20(4): 655-662, 2017 پmPubMedپn
- 3) Makiyama A, et al.: Gastric Cancer. 21(3): 464-472, 2018 پmPubMedپn
- 4) Kawakami T, et al.: Cancer Chemother Pharmacol. 78(4): 809-814, 2016 پmPubMedپn
GI cancer-net
ڈء‰»ٹيٹàژ،—أ‚جچLڈê
