FOLFIRI
 |
|
 |
|
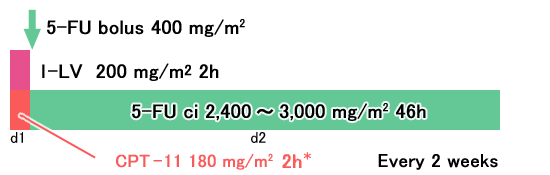
*CPT-11の日本での承認用量は150mg/m2、90min投与 |
|
Tournigand C, et al.: J Clin Oncol. 22(2): 229-237, 2004 |
|
ヨーロッパにおいて、LV/5-FU (5-FU持続点滴静注 de Gramont regimenあるいはAIO
regimen) にCPT-11を併用するphase IIIが行われ、RR、MST、TTPともにLV/5-FUより優れた成績が得られた1)。
2日間の5-FU持続静注+LVにCPT-11を併用するregimenをFOLFIRIと総称としているが、その後改良regimenとして、FOLFIRI 2、FOLFIRI
3が発表された。
■有効性
オリジナルのFOLFIRIについては、進行・再発大腸癌患者に対し、1st-line FOLFIRI→2nd-line FOLFOX 6でOS中央値21.5ヵ月、1st-line FOLFOX 6→2nd-line FOLFIRIでOS中央値20.6ヵ月と優れた成績が報告されている2) 。
FOLFIRI 2は、5-FU持続静注の後にCPT-11を投与する方法であり、5-FUとL-OHPの前治療を有する進行・再発大腸癌患者29例に対する奏効率は17% (5/29)、PFS中央値は4.1ヵ月、OS中央値は9.7ヵ月であった3)。なお、このregimenではhydroxyurea 1,500mgを3回投与する。
FOLFIRI 3は、FOLFOXを前治療に含む進行・再発大腸癌65例に対する奏効率が23%、PFS中央値が4.7ヵ月と報告された4)。このregimenでは、5-FU持続静注の前後にそれぞれCPT-11を投与する。
| FOLFIRI (1st-line) |
FOLFIRI2 (2nd-line) |
FOLFIRI3 (2nd-line) |
||
| 奏効率 (%) | 56 | 17 | 23 | |
| PFS中央値 (月) | 8.5 | 4.1 | 4.7 | |
| OS中央値 (月) | 21.5 | 9.7 | 10.5 | |
■安全性
オリジナルのFOLFIRIの1st-lineにおけるgrade 3/4有害事象では、発熱性好中球減少症、悪心・嘔吐、粘膜炎、疲労がFOLFOX6に比べて有意に多かった2)。
また、FOLFIRI2のgrade 3/4の有害事象としては、好中球減少が52%、下痢が31%にみられた。
FOLFIRI3のgrade 3/4の有害事象もFOLFIRI2と同様に、好中球減少、下痢、悪心・嘔吐の順に多くみられた4)。
Reference
GI cancer-net
消化器癌治療の広場
