悪心・嘔吐は、抗癌剤投与によって高い頻度で発現する非血液毒性の1つである。強い悪心・嘔吐は、しばしば食欲不振、脱水、低栄養、電解質異常などを引き起こし、抗癌剤投与の患者拒否やコンプライアンスの低下を招き、治療の継続が困難になることがある。薬物療法誘発悪心・嘔吐(chemotherapy-induced nausea and vomiting: CINV)は、使用する抗癌剤の種類、投与量そして投与経路によってその発現頻度が異なることが知られており1, 2)、がん薬物療法の成功のためには、この悪心・嘔吐を制御することが求められる。
発現機序
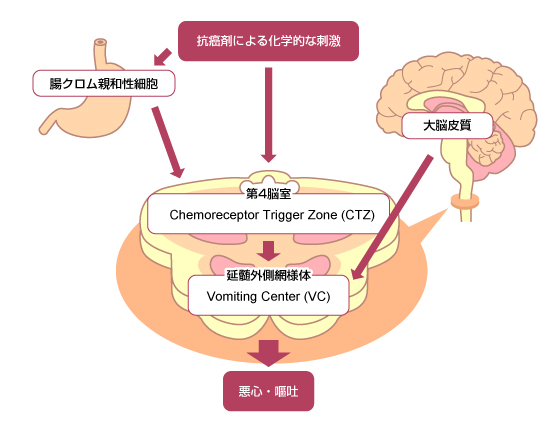
悪心・嘔吐は延髄外側網様体背側にある嘔吐中枢(vomiting center: VC)が刺激を受けて引き起こされると考えられている。がん薬物療法施行時においては、抗癌剤による化学的刺激が第4脳室の最後野に存在する化学受容器引き金帯(chemoreceptor trigger zone: CTZ)を直接刺激してVCへ刺激伝達される経路、消化管に存在する腸クロム親和性細胞からのセロトニン分泌等による上行性のCTZを刺激する経路、そして感情や感覚的な因子によって誘発される情動刺激によって大脳皮質からVCへ刺激が伝達される経路などが知られている (図1)3)。
さらにCTZやVCには、セロトニン(5-HT)、ヒスタミン、ドパミン、アセチルコリン、オピオイドなど様々な内因性神経伝達物質の受容体が存在することが知られている4)。
発現リスク
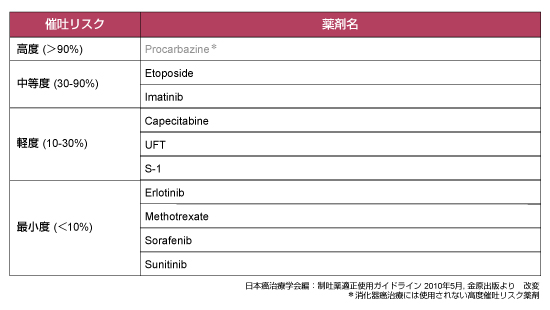
がん薬物療法で誘発される悪心・嘔吐の発現頻度は、使用する抗癌剤の催吐性に影響され、ASCO®やNCCN、MASCC等のガイドラインにおいてその程度を定義し分類されているが、統一はされていない。本邦においては、日本癌治療学会が作成した「制吐薬適正使用ガイドライン」において注射抗癌剤の催吐性リスク分類を行っており5)、実臨床においては最も有用であると考えられる。催吐性リスク分類では、制吐薬の予防投与無しで、各種抗癌剤投与後24時間以内に発症する悪心・嘔吐の割合に従い、高度、中等度、軽度、最小度の4つのカテゴリーに分類されている (表1)。また、経口抗癌剤に関しても同様に分類されており (表2)、その分類に合わせた予防制吐剤の適応が推奨されている。

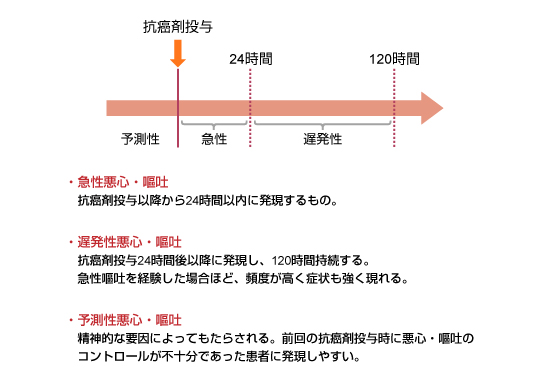
がん薬物療法による悪心・嘔吐は、その出現時期から急性、遅発性および予測性の3つに大別されている。急性の悪心・嘔吐は、『抗癌剤投与以降より24時間後までに生ずるもの』と定義されており、また遅発性の悪心・嘔吐は、『抗癌剤投与24時間以降120時間後までに生ずるもの』と定義されている (図2)。また、予測性の悪心・嘔吐は、抗癌剤による悪心・嘔吐を経験した患者において、実際の抗癌剤投与前から条件づけにより生じる。上記急性および遅発性の悪心・嘔吐は、ともに抗癌剤による直接的またはCTZを介した刺激によって生ずると考えられている。一方、予測性の悪心・嘔吐は、過去の抗癌剤投与による悪心・嘔吐の経験や情動的な感情の変化によって、大脳皮質からVCへ刺激が伝達されると考えられており、抗不安薬の予防投与が有効であるとされている6)。
悪心・嘔吐の重症度は、CTCAE v4.0が評価ツールとして汎用されており、実臨床における共通評価に繋がっている。ただ、この評価は、癌の治療法の安全性評価を容易にし、すべての癌領域での有害事象の記録や報告を標準化するために開発されたものであり、実地臨床が適切かどうかの監視や異なった有害事象の重症度の比較をすることは目的としていないため注意が必要である。
なお、悪心については、grade 1-3までの3段階、嘔吐についてはgrade 1-5までの5段階で設定されている (表3)。ただ、嘔吐は客観的評価が可能であるが、悪心はあくまでも主観であり、客観的な評価は困難であることに注意が必要である。
[CTCAE v4.03/MedDRA v12.0(日本語表記:MedDRA/J v16.0)対応-2013年4月9日]
![表3:CTCAE v4.0-JCOG[CTCAE v4.03/MedDRA v12.0(日本語表記:MedDRA/J v16.0)対応-2013年4月9日]](fukusayo_i/03/h_03.jpg)
催吐リスク毎に下記に示す。複数の薬剤が含まれる場合には、催吐リスクの高い薬剤の分類に従う。
- 高度催吐性リスク: CDDPを含むレジメン
- 中等度催吐性リスク: L-OHP、CPT-11を含むレジメン
- 軽度催吐性リスク: Gemcitabine 、5-FU、S-1、Capecitabineを含むレジメン
- 最小度催吐リスク: Panitumumab単剤、Cetuximab単剤
GI cancer-net
消化器癌治療の広場
