下痢とは、糞便が本来の固形状態ではなく、種々の要因で糞便中の水分量が増加し水様性になった状態で、1日の糞便中の水分量が200mL、または1日の糞便の重量が200gを超えるものと定義される。
下痢は患者のQOLを著しく低下させるだけでなく、治療困難や治療継続の拒否につながる。また、下痢が重症化すると、高度の脱水から腎不全、電解質異常、循環不全など、致死的な状況に至る危険性がある。さらに、好中球減少時に下痢が発症すると敗血症を続発する危険があるため、十分な対応が必要となる。
腸管粘膜上皮細胞は活発に分裂・増殖を繰り返しており、抗癌剤や放射線による障害を受けやすく、腸管粘膜上皮細胞の障害が下痢の主な原因となっている。下痢を起こしやすい抗癌剤として、Irinotecan (CPT-11)、フッ化ピリミジン系製剤、Cytarabine、Doxorubicin、Methotrexate (高用量) などが挙げられるが、特に消化器癌において投与されるCPT-11およびFluorouracil (5-FU) で発現頻度が高い。
CPT-11による下痢は、早発性の下痢と遅発性の下痢の2つに分類される。早発性の下痢は、CPT-11が有するコリン作動性によるものと考えられている。一方、遅発性の下痢はCPT-11の活性代謝物であるSN-38による消化管粘膜への直接的障害によるものと考えられている。すなわち、CPT-11は肝臓のカルボキシエステラーゼにより活性代謝物であるSN-38に変換された後、UDP-グルクロン酸転移酵素 (UGT) によりグルクロン酸抱合されたのち胆汁経由で腸管に排泄される (図1)。その後、腸内細菌のβ-グルクロニダーゼによって脱抱合を受け、再びSN-38となり腸管に直接的に障害を与え下痢を発現する。
5-FUはチミジンホスホリラーゼによりFdUMPに、オロテートホスホリボシルトランスフェラーゼ (OPRT) によりFUMPに代謝され、それぞれDNAおよびRNA合成を阻害することにより抗腫瘍活性を発揮するが、これらが腸管粘膜上皮細胞において作用すれば下痢を引き起こす。なお、S-1に含まれるオテラシルカリウムは消化管に分布し、OPRTを阻害することによって消化管におけるFUMP産生を阻害し、下痢の発現頻度を低下させると考えられている。
その他、癌患者の下痢の原因として、胃摘出手術後や開腹手術後、癌性腹膜炎による腸の癒着、腸内細菌叢の変化、薬剤性大腸炎、経管栄養剤、悪液質 (低栄養状態)、不安などの精神的要因がある。
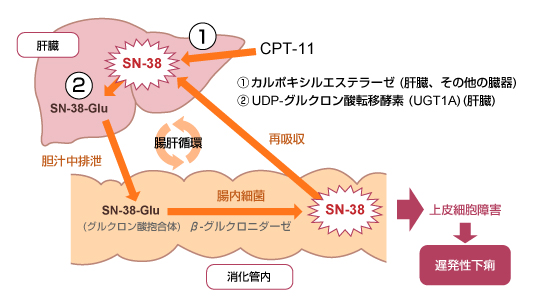
CPT-11による早発性の下痢は、投与中あるいは投与直後に発現し、多くは一過性である。遅発性の下痢は、投与24時間以降から2週間後にかけて出現し、持続することがある。
UGTには多くの遺伝子変異型 (一塩基多型) があり、UGT1A1*6 とUGT1A1*28 の変異がどちらもない場合の下痢発現率が14%に対して、どちらか一方がホモ接合体もしくは両者がヘテロ接合体としてある場合には20%であったことが報告されている1)。なお、15,385 例を対象とした市販後調査でのCPT-11による下痢発現率は43.0% (高度な下痢は10.2%) であった。
一方、5-FUによる下痢は、点滴静注後1週間から2ヵ月後に発現し、1,399例を対象とした市販後調査での下痢および軟便の発現頻度は9.5%であった2)。
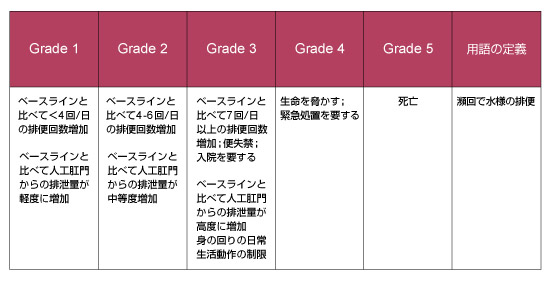
CTCAE v4.0の日本語訳JCOG版について表1示す。
- L-OHPベースのレジメン (FOLFOX ± Bevacizumab or Cetuximab or Panitumumab、FUFOX、
XELOX ± Bevacizumab) - CPT-11ベースのレジメン (CPT-11 ± S-1[IRIS、SIR] or Cetuximab or Panitumumab、FOLFIRI ± Cetuximab or Panitumumab、AIO + CPT-11、IFL ± Bevacizumab)
LV/UFT、Regorafenib単剤
GI cancer-net
消化器癌治療の広場
