FOLFIRI亄Bevacizumab
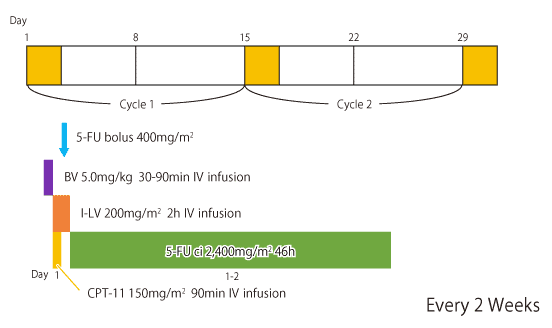 |
|
*CPT-11偺寢挵丒捈挵娻偵偍偗傞崙撪彸擣梡検偼150mg/m2偱偁傞丅偨偩偟丄搳梌検偼丄擭楊丄徢忬偵傛傝揔媂憹尭偡傞丅 |
Yamazaki K, et al.: Ann Oncol. 27(8): 1539-1546, 2016 |
Irinotecan乮CPT-11乯偼戝挵娻偵偍偗傞嶦嵶朎惈峈娻嵻偺key drug偱偁傝丄僼僢壔僺儕儈僕儞宯栻嵻偲條乆側暪梡椕朄偑峫埬偝傟丄尰嵼偱嵟傕桳岠惈偑崅偄CPT-11傪娷傫偩僼僢壔僺儕儈僕儞宯栻嵻偲偺doublet儗僕儊儞偼FOLFIRI椕朄偱偁傞丅V308乮GERCOR乯帋尡1)偵偍偄偰愗彍晄擻恑峴丒嵞敪戝挵娻偵懳偡傞1st-line偲偟偰丄FOLFOX偲FOLFIRI偺偳偪傜偐傜巊梡偟偰傕OS偵桳堄側嵎傪擣傔側偄偙偲偐傜1st-line偲偟偰FOLFIRI偼峀偔擣抦偝傟偰偄傞丅CPT-11偺妶惈懱偱偁傞SN-38偼娞憻撪偺uridine diphosphate glycosyl transferase 1A1乮UGT1A1乯偵傛傞僌儖僋儘儞巁書崌傪庴偗丄抇廯撪偵攔煏偝傟傞丅UGT1A1偵偼堚揱巕偺懡宆乮UGT1A1*6,*28乯偑懚嵼偟丄懡宆傪帩偨側偄姵幰傕偟偔偼1偮偺懡宆堚揱巕偺傒僿僥儘愙崌懱偱偁傞姵幰偵斾傋偰儂儌愙崌懱傕偟偔偼椉懡宆堚揱巕嫟偵僿僥儘愙崌懱偱偁偭偨応崌偵丄SN-38偺攔煏偑掅壓偟丄CPT-11偵傛傞暃嶌梡偑憹嫮偝傟傞丅偦偺偨傔丄CPT-11傪巊梡偡傞慜偵偼UGT1A1堚揱巕偺懡宆傪僠僃僢僋偡傞偙偲偑悇彠偝傟傞丅
仧WJOG4407G帋尡
愗彍晄擻恑峴丒嵞敪戝挵娻姵幰偵偍偗傞1st-line偲偟偰丄FOLFOX6亄Bevacizumab乮BV乯偵懳偟偰FOLFIRI亄BV偑旕楎惈偱偁傞偙偲傪専徹偟偨戞III憡帋尡偑峴傢傟偨2)丅揔奿徢椺402椺偑丄FOLFOX6亄BV孮偲FOLFIRI亄BV孮偵1丗1偺妱崌偱柍嶌堊壔妱傝晅偗偝傟偨丅
仭桳岠惈
庡梫昡壙崁栚偱偁傞PFS拞墰抣偼丄FOLFOX6亄BV孮10.7儠寧丄FOLFIRI亄BV孮12.1儠寧偱偁傝丄摉弶愝掕偝傟偨旕楎惈儅乕僕儞偱偁傞1.25傪壓夞傝丄FOLFOX6亄BV偵懳偟偰FOLFIRI亄BV偑旕楎惈偱偁傞偙偲偑徹柧偝傟偨乮p亖0.003乯丅杮帋尡偱偼丄旕楎惈偑専徹偝傟偨応崌偵FOLFOX6亄BV偵懳偡傞FOLFIRI亄BV偺桪墇惈傪夝愅偡傞偙偲偑pre-plan偝傟偰偄偨偨傔偵桪墇惈偺専摙傕峴傢傟偨偑丄FOLFIRI亄BV偺桪墇惈偼徹柧偝傟側偐偭偨乮p亖0.427乯丅傑偨丄暃師昡壙崁栚偱偁傞OS拞墰抣偼丄FOLFOX6亄BV孮30.1儠寧丄FOLFIRI亄BV孮31.4儠寧偱偁傝丄OS偵偍偄偰FOLFOX6亄BV偲FOLFIRI亄BV偼摨掱搙偱偁傞偙偲偑帵嵈偝傟偨丅憈岠妱崌偵偍偄偰傕FOLFOX6亄BV孮62%丄FOLFIRI亄BV孮64%偱偁傝丄椉孮偲傕摨摍偱偁偭偨丅
| FOLFOX6亄BV 乮n=200乯 |
FOLFIRI亄BV 乮n=202乯 |
HR 乮95% CI乯 |
P抣 | |
| 憈岠妱崌 | 62% | 64% | 亅 | 亅 |
| PFS拞墰抣 | 10.7儠寧 | 12.1儠寧 | 0.905 乮0.723-1.133乯 |
0.003 |
| OS拞墰抣 | 30.1儠寧 | 31.4儠寧 | 0.990 乮0.785-1.249乯 |
亅 |
仭埨慡惈
5%埲忋偺CTCAE grade乮埲壓grade乯3埲忋偺桳奞帠徾偼丄岲拞媴尭彮丄敀寣媴尭彮丄敪擬惈岲拞媴尭彮徢丄怘梸晄怳丄寫懹姶丄埆怱丒歲揻丄壓棢丄枛徑惈姶妎僯儏乕儘僷僠乕丄惷柆寣愷徢偱偁偭偨丅grade 3埲忋偺岲拞媴尭彮乮45% vs. 35%, p亖0.031乯偲敀寣媴尭彮乮11% vs. 5%, p亖0.014乯偼FOLFIRI亄BV孮偱桳堄偵昿搙偑崅偐偭偨偺偵懳偟偰丄grade 3埲忋偺枛徑惈姶妎僯儏乕儘僷僠乕乮22% vs. 0%, p亙0.001乯偼FOLFOX6亄BV孮偱桳堄偵昿搙偑崅偐偭偨丅桳奞帠徾偵傛偭偰帋尡帯椕偑宲懕崲擄偲側偭偨姵幰偺妱崌偼丄FOLFOX6亄BV孮33%丄FOLFIRI亄BV孮27%偱丄椉孮偲傕偵摨掱搙偱偁傝丄FOLFIRI亄BV儗僕儊儞偼桳岠惈丒埨慡惈偲傕偵愗彍晄擻恑峴丒嵞敪戝挵娻偵懳偡傞1st-line偲偟偰桳梡偱偁傞偙偲偑帵偝傟偨丅
杮帋尡偱偼丄暃師揑昡壙崁栚偲偟偰FACT乮functional assessment of cancer therapy乯傪梡偄偨QOL偺挷嵏偑幚巤偝傟偨丅摿偵恄宱忈奞撆惈偵懳偟偰丄FACT/GOG-Ntx偺neurotoxicity subscale 11崁栚傪梡偄偰昡壙偝傟丄帋尡帯椕奐巒偐傜18儠寧帪揰偱FOLFOX6亄BV孮偱偼FOLFIRI亄BV孮偵斾傋偰丄偟傃傟偵傛偭偰QOL傪桳堄偵掅壓偝偣傞偙偲偑帵偝傟偨乮p亙0.001乯丅Oxaliplatin偺搳梌宲懕婜娫拞墰抣偑5.1儠寧偱偁偭偨偙偲偐傜悇應偟偰傕丄FOLFOX6亄BV儗僕儊儞偱偼挿婜偵枛徑惈姶妎僯儏乕儘僷僠乕偑巆懚偡傞偙偲偵傛偭偰QOL偑掅壓偡傞偙偲偵拲堄偡傋偒偱偁傞丅堦曽丄FOLFIRI亄BV偼CPT-11偺搳梌宲懕婜娫拞墰抣偑8.5儠寧偱偁傝丄壓棢傗岲拞媴尭彮側偳偵懳偡傞暃嶌梡儅僱僕儊儞僩傪偟偭偐傝峴偊偽丄QOL傪曐偪側偑傜挿婜偵巊梡壜擻側儗僕儊儞偱偁傞偲偄偊傞丅
儗僕儊儞夝愢幏昅丗惞儅儕傾儞僫堛壢戝妛 椪彴庮釃妛島嵗丂埳郪 捈庽 愭惗
References
GI cancer-net
徚壔婍娻帯椕偺峀応
