瀧内:GISTに対するCTによるフォローアップの間隔はどのくらいが適切でしょうか。
久保田:今回、策定された日本版GISTガイドラインのGIST治療マニュアルでは「4〜6ヵ月ごとのCTによるフォローアップ」としています。本ガイドラインは、GIST研究会の要請により日本胃癌学会と日本癌治療学会が合同で策定しました。主にNCCNのガイドラインとESMOの勧告を参考にしています。
瀧内:日本版GISTガイドラインに準拠すると、今回の症例にはどのように対処すべきでしょうか。
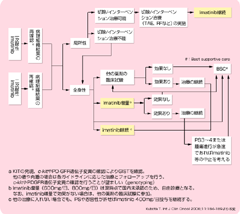
久保田:最初に述べたように、imatinib 400mg/日が副作用で継続不能となった症例ですので、本ガイドラインによれば次なる選択肢は新規薬剤の臨床試験となります。あるいはbest supportive careしかありません。NCCNのガイドラインとESMOの勧告でも、PDをfailureと考えると次なる選択肢は臨床試験というのが現状と思います。
瀧内:残念ながらGIST治療の選択肢は限られたものしかないのが現状ですね。それでは、新規薬剤についてはいかがでしょうか。現在、マルチターゲットの血管内皮増殖因子(VEGF)阻害薬であるsunitinib(SU11248)、AMG706などの開発が進められています。
|
佐藤:Sunitinibは本邦での第II相試験が順調に進んでいます。安全性の詳細はわかりませんが、海外でのデータも合わせて、有効性においては十分に期待できるものと考えております。
瀧内:次に、imatinib抵抗性GISTへの対処法についてはいかがでしょう。imatinibを増量するというアプローチもあるようですが。
久保田:Imatinib 400mg/日の抵抗性例に対するimatinib増量(600mg/日)の有効性は無作為化臨床試験で証明されています。
大村:その場合、問題となるのは保険の適用ですね。日本では400mg/日までしか承認されていませんので適応外になります。
瀧内:治療選択肢が限られている日本の現状では、今後の可能性としては新規薬剤の臨床試験とimatinibのdose escalation試験ということになりますか。
大村:臨床試験に登録されるのはきわめて限られた症例だけですから、実地臨床では査定を覚悟のうえで何とか用量を上げるという方策しかないと考えます。
佐藤:確かにexon 9の異常に限定すれば可能性はあると思いますが、imatinib 800mg/日と400mg/日の比較では有意差が出ていませんので、増量は必ずしもよくないという意見もあるようです。
瀧内:しかし、抵抗性例の中には増量によって効果がみられる症例もあるわけですから、試みる価値はあるといってよいでしょう。また、imatinib抵抗性例に対するsecond lineとしてのsunitinibは、PRが13%、6ヵ月以上持続したPR+SDが42%と有望な成績が報告されており、期待が高まっています。