S-1+Docetaxel(DTX)
 |
 |
|
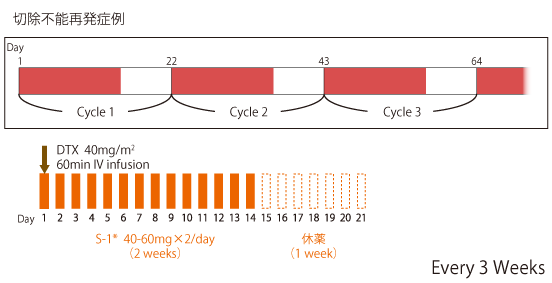
*S-1の1日投与量は体表面積(m2)により調整 |
Koizumi W, et al.: J Cancer Res Clin Oncol. 140(2): 319-328, 2014 |
S-1+DTXは、第III相試験(START試験)においてS-1単剤投与群と比較し無増悪生存期間(PFS)の有意な延長および安全性が示された。切除不能・進行胃癌の1stラインの標準治療はフッ化ピリミジン製剤と白金製剤の併用療法であり、S-1+DTX療法は白金製剤が使えない場合など、条件付きで推奨されるレジメンという位置付けとなる。また、Stage III根治切除胃癌に対する術後補助化学療法として推奨されるレジメンである。
◆START試験1)
切除不能の再発進行胃癌に対する1次治療として、S-1単剤群(n=321)に対するS-1+DTX併用群(n=314)の優越性を検証した第III相試験である。
◆JACCRO GC-07(START-2)試験2)
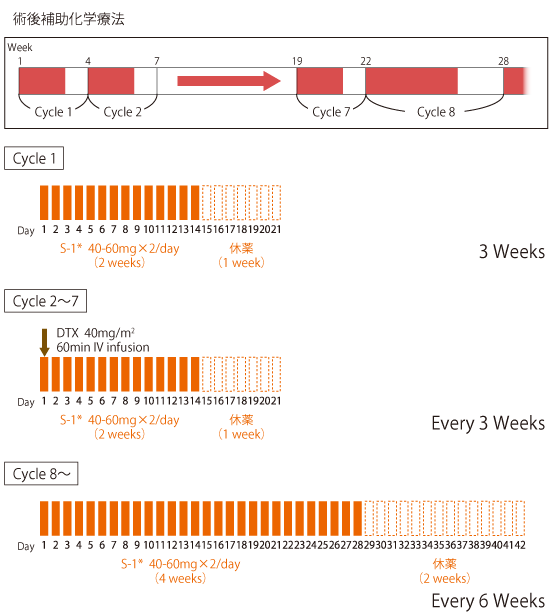
根治切除後Stage III胃癌に対する、術後補助化学療法としてのS-1群に対するS-1+DTX併用群の優越性を検証した第III相試験である。S-1+DTX療法では、1年間のS-1内服に対し、2コースより7コースまでDTXを併用し、以後再びS-1単独で継続する投与法がとられた。
■有効性
START試験1)の観察察期間中央値は11.4ヵ月であった。主要評価項目である生存期間(OS)の中央値は、S-1+DTX群で12.5ヵ月、S-1群で10.8ヵ月であり(HR=0.84、95% CI: 0.71-0.99、p=0.032)、S-1+DTXの優越性が示された。副次評価項目については、PFSにおいてS-1+DTX群で中央値5.3ヵ月、S-1群で4.2ヵ月となりS-1+DTX群において有意な延長が認められた(HR=0.77、95% CI: 0.65-0.90、p<0.001)。また、測定可能病変例における奏効割合(ORR)はS-1+DTX群で38.8%、S-1群で26.8%であり有意差を認めた(p=0.005)。測定不能病変例に対するサブグループ解析では、S-1+DTX群のPFS 8.4ヵ月に対してS-1群で5.6ヵ月(HR=0.613、95% CI: 0.435-0.862、p=0.0045)、OSがS-1+DTX群の17.9ヵ月に対してS-1群で12.0ヵ月(HR=0.649、95% CI: 0.461-0.914、p=0.0127)と、よりS-1+DTXが効果的であることが示唆された。
JACCRO GC-07試験2)の主要評価項目である3年無再発(RFS)生存割合は、S-1+DTX群の65.9%に対してS-1群では49.5%(HR=0.632、99.99% CI: 0.400-0.998、p=0.0007)とS-1+DTX群で有意に良好であったことから、2017年9月をもって本試験は有効中止となっている。サブグループ解析では、年齢や性別、pStage(IIIA/IIIB/IIIC)などの特定の集団との明らかな交互作用は認めなかった。
| START試験 | S-1+DTX群 | S-1群 | HR (95% CI) |
P値 |
| OS | 12.5ヵ月 | 10.8ヵ月 | 0.84 (0.71-0.99) |
0.032 |
| PFS | 5.3ヵ月 | 4.2ヵ月 | 0.77 (0.65-0.90) |
<0.001 |
| ORR | 38.8% | 26.8% | - | 0.005 |
| JACCRO GC-07試験 | S-1+DTX群 | S-1群 | HR (99.99% CI) |
P値 |
| 3年RFS割合 | 65.9% | 49.5% | 0.632 (0.400-0.998) |
0.0007 |
■安全性
START試験1)におけるGrade 3以上の有害事象は、S-1+DTX群において58.1%、S-1群では39.6%とS-1+DTX群で有意に多かった(p<0.001)。このうち、好中球減少および白血球減少といった血液毒性のほか、発熱性好中球減少症(2.9%)も同様に高かったことから感染が問題となるため、発熱時に熱源検索および適切な抗菌薬の開始を検討すべきである。また、本研究において頻度の記載はないがDTXを投与することで高率に脱毛がみられるため、治療開始前に言及しておく必要がある。
JACCRO GC-07試験2)におけるGrade 3以上の有害事象は、S-1+DTX群がS-1群に対して好中球減少(38.1% vs. 16.1%)、発熱性好中球減少症(4.7% vs. 0.3%)と血球減少に起因する毒性が高かった。All gradesの非血液毒性としては、倦怠感(51.9% vs. 35.9%)や脱毛(57.8% vs. 3.4%)がS-1+DTX群において高く、さらに両群での頻度は同程度であるが、S-1による粘膜障害として口腔粘膜炎および下痢も比較的高頻度(Grade 3以上が2.0〜8.9%)で認められた。
START試験1)の結果より、切除不能の再発進行胃癌に対してS-1+DTXは、白金製剤を用いることができない症例や、標的病変を有さない腹膜転移症例などに対する、条件付きで推奨されるレジメンと考えられている。
JACCRO GC-07試験2)の結果より、S-1+DTX療法は、Stage III根治切除胃癌に対する、術後補助化学療法として推奨されるレジメンの一つと考えられる。もう一つの標準的術後化学療法である、フッ化ピリミジン製剤とOxaliplatinとの併用療法との優劣は不明であるが、毒性やスケジュール、患者の希望などを考慮して決定されるべきである。
レジメン解説執筆:国立がん研究センター中央病院 内視鏡科 伊藤 卓彦 先生
References
GI cancer-net
消化器癌治療の広場
