Infusional 5-FU/LVپ{Bevacizumabپisimplified LV5FU2پ{Bevacizumabپj
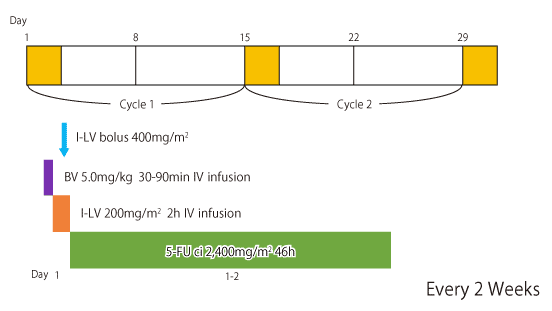 |
Kabbinavar FF, et al.: J Clin Oncol. 23(16): 3706-3712, 2005 |
Simplified LV5FU2پisLV5FU2پj‚حde Gramont regimenپiclassic LV5FU2: cLV5FU2پj‚و‚è2“ْ–ع‚جLeucovorinپiLVپj‚ئ5-FU‚ج‹}‘¬گأ’چ‚ًڈب‚«پA1“ْ–ع‚ج5-FUژ‘±گأ’چ‚ً46ژٹش“ٹ—^‚ة‚µ‚½ٹب—ھ‚ب“ٹ—^ƒXƒPƒWƒ…پ[ƒ‹‚إ‚ ‚éپBsLV5FU2‚حپAOxaliplatin‚âIrinotecanپiCPT-11پj‚ئ•¹—p‚µ‚½FOLFOX6پAFOLFIRI‚ئ‚µ‚ؤژ{چs‚³‚ê‚邱‚ئ‚ھ‘½‚¢پBsLV5FU2‚ئBevacizumabپiBVپj‚ً•¹—p‚µ‚½‘OŒü‚«‚بŒ‹‰ت‚ح‘¶چف‚µ‚ب‚¢‚à‚ج‚جپAFOLFOX6پAFOLFIRI‚ةBV‚ًڈمڈو‚¹‚·‚邱‚ئ‚ج—LŒّگ«پEˆہ‘Sگ«‚ھ‘½‚‚جژژŒ±‚ة‚ؤ•ٌچگ‚³‚ê‚ؤ‚¨‚èپAsLV5FU2پ{BV‚جˆہ‘Sگ«‚ح’S•غ‚³‚ê‚é‚à‚ج‚ئچl‚¦‚ç‚ê‚éپB‚½‚¾‚µپA‘ه’°ٹàگf—أƒKƒCƒhƒ‰ƒCƒ“‚إ‚حپAچ‚—îژز‚â‘ںٹي‹@”\ڈلٹQ‚ً—L‚µپA‹—ح‚بژ،—أ‚ھ“K‰‚ئ‚ب‚ç‚ب‚¢ٹ³ژز‚ة‘خ‚µ‚ؤپAsLV5FU2پ{BVƒŒƒWƒپƒ“‚ھگ„ڈ§‚³‚ê‚ؤ‚¢‚éپBFOLFOX6پ{BVپAFOLFIRIپ{BV‚ج—صڈ°ژژŒ±‚إ‚حپAچ‚—îژزپi“ء‚ة75چخˆبڈمپj‚ً‘خڈغ‚ئ‚µ‚ؤ‚¢‚ب‚¢‚±‚ئ‚ھ‘½‚پAچ‚—îژز‚ة‘خ‚·‚ésLV5FU2پ{BVƒŒƒWƒپƒ“‚جˆہ‘Sگ«‚ئ—LŒّگ«‚ھŒœ”O‚³‚ê‚éپB
پںFFCDژژŒ±
75چخˆبڈم‚جگطڈœ•s”\گiچsپEچؤ”‘ه’°ٹàٹ³ژز‚ً‘خڈغ‚ئ‚µ‚ؤپA1st-line‚ة‚¨‚¯‚écLV5FU2‚à‚µ‚‚حsLV5FU2‚ة‘خ‚µ‚ؤCPT-11‚جڈمڈو‚¹Œّ‰ت‚ًŒں“¢‚µ‚½‘وIII‘ٹژژŒ±‚إ‚ ‚é1)پB4ŒQ‚جƒRƒzپ[ƒg‚ھ‚ ‚èپA“Kٹiڈا—ل282—ل‚ھپAcLV5FU2ŒQ‚ئsLV5FU2ŒQپAcLV5FU2پ{CPT-11ŒQ‚ئFOLFIRIŒQ‚ة1پF1پF1پF1‚جٹ„چ‡‚إ–³چىˆ×‰»ٹ„‚è•t‚¯‚³‚ꂽپB
پںAVF0780gژژŒ±/AVF2192gژژŒ±/AVF2107gژژŒ±‚ج“چ‡‰ًگح
گطڈœ•s”\گiچsپEچؤ”‘ه’°ٹàٹ³ژز‚ً‘خڈغ‚ئ‚µ‚ؤپA1st-line‚ة‚¨‚¯‚éRPMIپiRoswell Park Memorial Instituteپj‚ـ‚½‚حbolus 5-FU/LVپ{CPT-11پiIFLپj‚ة‘خ‚µ‚ؤRPMIپ{BV‚ج—LŒّگ«‚ًŒں“¢‚µ‚½3‚آ‚جƒ‰ƒ“ƒ_ƒ€‰»”نٹrژژŒ±‚ًƒپƒ^‰ًگح‚µ‚½Œ‹‰ت‚ھ•ٌچگ‚³‚ꂽ2)پBRPMI‚ـ‚½‚حIFLŒQ241—ل‚ة‘خ‚µ‚ؤRPMIپ{BVŒQ249—ل‚إ‚ ‚ء‚½پB
‚±‚ê‚ç‚جژژŒ±Œ‹‰ت‚ً‚à‚ئ‚ةپAcLV5FU2‚ئsLV5FU2‚ج“¯“™گ«پAFUگ»چـ‚ةBV‚ً•¹—p‚·‚邱‚ئ‚ج—LŒّگ«‚ئˆہ‘Sگ«‚ة‚آ‚¢‚ؤŒں“¢‚·‚éپB
پ،—LŒّگ«
FFCDژژŒ±‚جژه—v•]‰؟چ€–ع‚حLV5FU2ŒQ‚ئCPT-11ŒQ‚ة‚¨‚¯‚éPFS‚ج’†‰›’l‚ب‚ç‚ر‚ةپACLASSICŒQپicLV5FU2 or cLV5FU2پ{CPT-11پj‚ئSIMPLIFIEDŒQپisLV5FU2 or FOLFIRIپj‚ة‚¨‚¯‚éPFS‚ج’†‰›’l‚إ‚ ‚éپBLV5FU2ŒQ5.2ƒ•ŒژپACPT-11ŒQ7.3ƒ•Œژ‚إ‚ ‚èپA—¼ŒQ‚إ—Lˆسچ·‚ً”F‚ك‚ب‚©‚ء‚½پipپپ0.15پjپB“¯—l‚ةCLASSICŒQ6.5ƒ•ŒژپASIMPLIFIEDŒQ6.0ƒ•Œژ‚إپA—Lˆسچ·‚ً”F‚ك‚ب‚©‚ء‚½پipپپ0.19پjپBcLV5FU2‚ئsLV5FU2‚إƒTƒuƒOƒ‹پ[ƒv‰ًگح‚ھ‚ب‚³‚êپAPFS’†‰›’l‚حcLV5FU2 4.71ƒ•ŒژپAsLV5FU2 5.29ƒ•Œژ‚إ‚ ‚èپA“¯’ِ“x‚إ‚ ‚ء‚½پB
| LV5FU2ŒQ پin=142پj |
CPT-11ŒQ پin=140پj |
HR پi95% CIپj |
P’l | |
| PFS’†‰›’l | 5.2ƒ•Œژ | 7.3ƒ•Œژ | 0.84 پi0.66-1.07پj |
0.15 |
| OS’†‰›’l | 14.7ƒ•Œژ | 14.9ƒ•Œژ | 0.96 پi0.75-1.24پj |
0.77 |
| CLASSICŒQ پin=141پj |
SIMPLIFIEDŒQ پin=141پj |
HR پi95% CIپj |
P’l | |
| PFS’†‰›’l | 6.5ƒ•Œژ | 6.0ƒ•Œژ | 0.85 پi0.67-1.09پj |
0.19 |
| OS’†‰›’l | 15.2ƒ•Œژ | 11.4ƒ•Œژ | 0.71 پi0.55-0.92پj |
0.01 |
“چ‡‰ًگح‚جژه—v•]‰؟چ€–ع‚حOS’†‰›’l‚إ‚ ‚èپARPMI‚à‚µ‚‚حIFLŒQ14.6ƒ•Œژ‚ئRPMIپ{BVŒQ17.9ƒ•Œژ‚إ‚ ‚èپARPMIپ{BVŒQ‚إ—Lˆس‚ب‰„’·‚ً”F‚ك‚½پipپپ0.0081پjپB‚ـ‚½پAPFS’†‰›’l‚àRPMI‚à‚µ‚‚حIFLŒQ5.6ƒ•Œژ‚ئRPMIپ{BVŒQ8.8ƒ•Œژ‚إ‚ ‚èپipپ…0.0001پjپA‘tŒّٹ„چ‡‚àRPMI‚à‚µ‚‚حIFLŒQ24.5%‚ئRPMIپ{BVŒQ34.1%‚ئRPMIپ{BVŒQ‚إ—Lˆس‚إ‚ ‚ء‚½پipپپ0.019پjپB
| RPMI/IFL پin=241پj |
RPMIپ{BV پin=249پj |
HR پi95% CIپj |
P’l | |
| ‘tŒّٹ„چ‡ | 24.5% | 34.1% | پ| | 0.019 |
| PFS’†‰›’l | 5.6ƒ•Œژ | 8.8ƒ•Œژ | 0.63 پi0.5-0.78پj |
0.0001 |
| OS’†‰›’l | 14.9ƒ•Œژ | 17.9ƒ•Œژ | 0.74 پi0.59-0.93پj |
0.0081 |
پ،ˆہ‘Sگ«
FFCDژژŒ±‚ة‚¨‚¢‚ؤCTCAE gradeپiˆب‰؛gradeپj3ˆبڈم‚ج—LٹQژ–ڈغ”Œ»ٹ„چ‡‚حLV5FU2ŒQ52.2%پACPT-11ŒQ76.3%‚ئCPT-11•¹—pregimen‚إچ‚‚¢Œ‹‰ت‚إ‚ ‚ء‚½پB“ء‚ةپACPT-11ŒQ‚إ‚حچD’†‹…Œ¸ڈپi5.2% vs. 38.5%پjپA””Mگ«چD’†‹…Œ¸ڈڈاپi0.7% vs. 7.4%پjپAˆ«گSپi1.5% vs. 6.7%پjپAڑq“fپi1.5% vs. 5.9%پjپA‰؛—ںپi5.2% vs. 22.2%پjپAŒŒگًڈاپi3.0% vs. 8.9%پj‚ھچ‚‚¢‚±‚ئ‚ھژ¦‚³‚ꂽپBCLASSICŒQ‚ئSIMPLIFIEDŒQ‚إ—LٹQژ–ڈغ‚ج”Œ»•p“x‚ة—Lˆس‚بچ·‚ً”F‚ك‚ب‚©‚ء‚½پB
“چ‡‰ًگحژژŒ±‚إ‚حپARPMI‚à‚µ‚‚حIFLŒQ‚ئ”نٹr‚µ‚ؤRPMIپ{BVŒQ‚ة‚¨‚¢‚ؤپAgrade 3ˆبڈم‚جچ‚ŒŒˆ³‚ج•p“x‚ھڈمڈ¸‚µ‚½‚ھپi3% vs. 16%پjپA‚»‚ج‘¼‚ج—LٹQژ–ڈغ‚ة‚¨‚¢‚ؤ—Lˆس‚بچ·‚ً”F‚ك‚ب‚©‚ء‚½پB
ˆبڈم‚ج‚±‚ئ‚©‚çپAچ‚—îژز‚â‘ںٹي‹@”\ڈلٹQ‚ً—L‚µپA‹—ح‚بژ،—أ‚ھ“K‰‚ئ‚ب‚ç‚ب‚¢گطڈœ•s”\گiچsپEچؤ”‘ه’°ٹàٹ³ژز‚ج1st-line‚ئ‚µ‚ؤپAsLV5FU2پ{BV‚ح‘I‘ًژˆ‚جˆê‚آ‚ئ‚ب‚蓾‚é‚ئچl‚¦‚ç‚ê‚éپB
ƒŒƒWƒپƒ“‰ًگàژ·•MپFگ¹ƒ}ƒٹƒAƒ“ƒiˆم‰ب‘هٹw —صڈ°ژîل‡ٹwچuچہپ@ˆةàV ’¼ژ÷ گوگ¶
References
- •›چى—p‘خچôچuچہپuˆ«گSپEڑq“fپv
- •›چى—p‘خچôچuچہپu‰؛—ںپv
GI cancer-net
ڈء‰»ٹيٹàژ،—أ‚جچLڈê
