
転移性大腸癌において、1st-lineの効果が得られた症例での最適な投与継続期間および継続する治療内容 (休薬または一部の薬剤を継続する) については、controversialである。
XELOX+bevacizumab療法を6サイクル施行後、bevacizumab単剤投与による維持療法の有効性と忍容性を評価する目的で、非劣性デザインの多施設共同無作為化比較第III相試験が行われた。
前治療歴のない転移を有する大腸癌に対し、XELOX+bevacizumab療法 [capecitabine (1,000mg/m2、1日2回投与、day1-14) +oxaliplatin (130mg/m2、day1) +bevacizumab (7.5mg/kg、day1投与)、3週毎投与] 6サイクル実施後に、増悪が認められるまで同治療を継続する群 (Arm A) とbevacizumab単剤投与を維持療法として継続する群 (Arm B) に無作為に割り付けた。
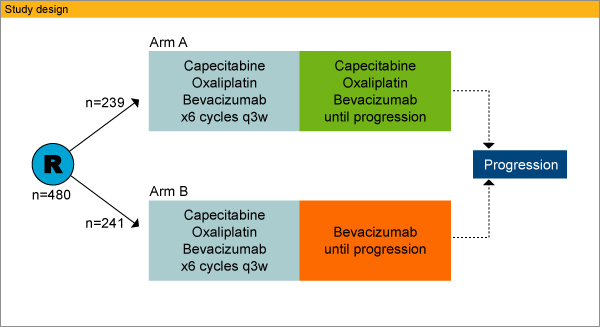
・二次エンドポイント:overall survival (OS)、objective response rate (ORR)、安全性など
480症例が無作為に割り付けられ、Arm Aは239例、Arm Bは241例であった。一次エンドポイントであるPFS中央値はArm Aが10.4ヵ月、Arm Bが9.7ヵ月、HRは1.11 (0.89-1.37) で、非劣性は証明されなかった。ORR、PFS、OSのいずれも2群間に統計学的な有意差は認めなかった。
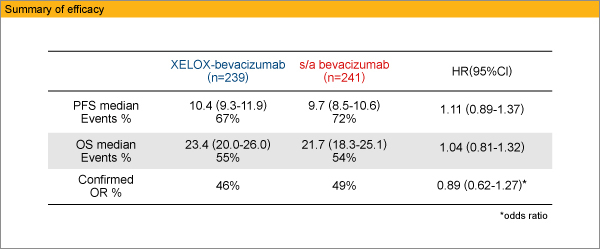
Grade 3/4の有害事象は、下痢 (Arm A/Arm B:10.9%/13.9%)、手足症候群 (12.2%/6.7%)、神経障害 (24.8%/7.6%)、倦怠感 (10.5%/4.2%)、高血圧 (3.8%/7.1%) などであり、特に手足症候群と末梢神経障害の発症が抑えられた。
非劣性は証明できなかったが、XELOX+bevacizumab療法後の維持療法としてのbevacizumab単剤投与は、従来行われているXELOX+bevacizumab療法を継続する治療に比べて劣っていないことが示された。
本研究より、bevacizumab単剤投与による維持療法が転移再発大腸癌患者に対するXELOX+bevacizumab療法中の適切な治療オプションであることが示唆された。
本報告のポイントは、維持治療のあり方である。大腸癌の標準療法であるFOLFOX療法の場合は、oxaliplatinによる末梢神経毒性、さらにXELOX療法では、capecitabineによる手足症候群が、累積薬剤投与量により問題化する。このような薬剤特異性のある副作用が発現したときは、併用療法のすべての薬剤を中止するのではなく、問題となる薬剤のみを減量、中止とすることが実臨床でのコンセンサスとなりつつある。
一方、OPTIMOX試験の報告以来、本試験のような特定の薬剤を予め計画的に休止する維持治療が注目されている。ただし、休止する薬剤により副作用軽減が図れるのだが、抗腫瘍効果も減弱するため、病勢の抑制力が問題になる。本試験では、bevacizumab単独のみにその効果を期待しているが、bevacizumabはすでにこれまでの試験で、単剤よりは細胞毒性のある抗癌剤との併用が推奨されている。
本試験の結果は、bevacizumab単剤の維持療法を強く推奨するまでのインパクトはない。ただし、capecitabine、oxaliplatinなどの毒性が問題となる症例においてbevacizumab単剤を使用する妥当性は示している。今後は、DREAM、CAIRO-3、AIO-ML2176試験などの結果を待つ。
(レポート:松阪 諭 監修・コメント:佐藤 温)