
転移性大腸癌患者における治療のゴールは、palliativeから腫瘍縮小による外科的切除の適応による生存期間の延長へと大きくシフトしつつある。Panitumumab (Pmab) は完全ヒト型抗EGFRモノクローナル抗体であり、転移のある進行再発大腸癌患者の1st-lineにおけるFOLFOX療法への併用、または2nd-lineにおけるFOLFIRI療法への併用に対する上乗せ効果が大規模第III相試験ですでに証明されている。今回、Pmabの1st-lineとしてのFOLFIRI療法への併用についてのオープンラベル単アーム多施設共同第II相試験 (20060314) の結果から、切除率のデータについて報告する。
対象は、RECISTにより組織学的に転移が判定されている、化学療法の治療歴がない、ECOG PS 0-2、切除組織でバイオマーカーが測定可能であるという条件を満たす転移のある大腸癌とした。
治療は、Pmab (6mg/kg) +FOLFIRI療法を2週間毎に施行した (2029年 米国臨床腫瘍学会年次集会, #4085参照)。
一次エンドポイントは奏効率 (ORR ; objective response rate)、二次エンドポイントはprogression-free survival (PFS)、安全性などとした。
登録患者数は154例であり、一次解析 (2009年6月) の時点で全体の94% (n=145) の症例でKRASが測定可能であった。そのうち86例 (59%) がKRAS野生型、59例 (41%) が変異型であった。KRAS野生型およびKRAS変異型で、男性の割合は各々78%、54%、年齢中央値は63.5歳、65.0歳、ECOG PS 0-1が95%、93%であった。
ORRはKRAS野生型56% (CR : 2例、PR : 46例)、変異型38% (CR : 1例、PR : 21例)、PFS中央値は8.9ヵ月、7.2ヵ月であった。転移巣の切除を行ったのは19例で、Pmab最終投与から手術までの期間中央値は43日 (95%CI : 16-101) であった。切除を行った患者のうち5例は術後に再度Pmabが投与された。切除から再投与までの期間中央値は48日 (95%CI : 28-168) であった。
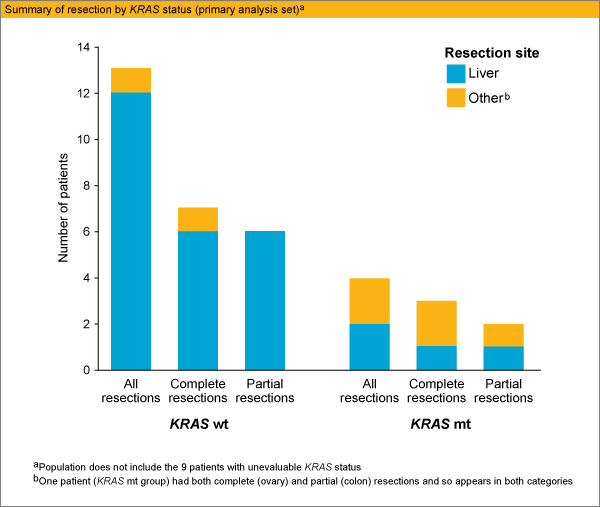
両群の切除率はKRAS野生型15% (95%CI : 8.3-24.5)、変異型7% (95%CI : 1.9-16.5) であった。切除部位の大半は肝臓で (92%、50%)、肝転移のみの症例52例に限定すれば、切除率は全体で29% (15例 : KRAS判定不能例も含む)、KRAS野生型で35% (11例/31例中)、KRAS変異型で13% (2例/16例中) であった。その他の切除部位としては、KRAS野生型で皮膚転移1例、KRAS変異型で卵巣および結腸1例、肺転移が1例認められた。
転移巣の完全切除率 (R0) は、KRAS野生型が8% (7例/86例中、95% CI : 3.3-16.1)、変異型が5% (4例/59例中、95% CI : 1.1-14.2) であった。
有害事象についてはKRAS野生型および変異型で相違は認められなかった。手術に関連した有害事象は5例で、創傷治癒遅延はみられなかった。5例の内訳は、術後痛3例、全身状態の悪化1例、下大静脈血栓症1例であった。
一次治療としてのPmab+FOLFIRI療法は十分に忍容できるレジメンである。また、抗EGFR治療におけるKRAS status別の効果への影響は従来の報告と同様であり、本試験においてもKRAS野生型で良好な成績が得られた。
2009年の米国臨床腫瘍学会年次集会で報告された中間解析 (2029年 米国臨床腫瘍学会年次集会, #4085) の続報である。KRASの解析症例が3例加えられており、有害事象の詳細はそちらを参照されたい。KRAS statusと有害事象の発現率との間には関連がないと報告されているが、KRAS statusは腫瘍組織に限ったものであるから当然と言える。また、今回の解析から、Pmab+FOLFIRI療法は、KRAS野生型大腸癌において、その転移巣、特に肝転移における完全切除を可能にするpotentialを有するものと考えられた。
(レポート:家接 健一 コメント:大村 健二)