

これまでEGFR阻害薬のバイオマーカー候補としてEGFRの発現が検討されてきたが、腫瘍細胞の免疫組織化学染色 (IHC) におけるEGFR発現とEGFR阻害薬の抗腫瘍効果とはほとんど関係ないと報告されている1-2)。しかしながら、現在も治療前には腫瘍組織を採取し、検査を実施しているのが実状である。今回、抗EGFR抗体panitumumab (Pmab) の2つの無作為化比較第III相試験のデータをEGFR発現の有無によって解析した結果が報告された。
1) Hecht JR, et al.: Clin Cancer Res. 2010; 16: 2205-2213
2) Chung KY, et al.: J Clin Oncol. 2005; 23: 1803-1810
| ◆ | 対象 | ||
| 20050181試験 (#3565)、PRIME試験 (#3566) に登録されたKRAS野生型の症例 | |||
| ◆ | 検討項目 | ||
| ・ | 効果予測因子としての検討 |
: | 免疫組織化学染色におけるEGFR発現の有無によるPmab併用群および非併用群のprogression-free survival (PFS)、overall survival (OS)、奏効率 (objective response rate:ORR) |
| ・ | 予後予測因子としての検討 | : | 免疫組織化学染色におけるEGFR発現の有無によるPmab非併用群のPFS、OS、ORR |
| ◆ | 検査方法 | ||
| Dako EGFR pharmDXTM kitを使用 | |||
◆20050181試験 (#3565)
KRAS野生型でかつEGFRの評価が可能であった症例は、FOLFIRI+Pmab療法群で198例[EGFR陽性 (+) 148例、EGFR陰性 (-) 50例]、FOLFIRI療法群で193例[EGFR (+) 147例、EGFR (-) 46例]であった。
PFS中央値は、EGFR (+) ではFOLFIRI+Pmab療法群で6.4ヵ月、FOLFIRI療法群で5.1ヵ月 (HR=0.80、95%CI:0.62-1.03、p=0.09)、EGFR (-) では各々7.5ヵ月、5.5ヵ月 (HR=0.81、95%CI:0.50-1.31、p=0.40) であった。
OS中央値は、EGFR (+) でFOLFIRI+Pmab療法群14.1ヵ月、FOLFIRI療法群12.8ヵ月 (HR=0.87、95%CI:0.65-1.15、p=0.32)、EGFR (-) で各々14.5ヵ月、12.5ヵ月 (HR=0.87、95%CI:0.53-1.43、p=0.58) であった。ORRは、EGFR (+) で34%、13%、EGFR (-) では51%、7%であった。
◆PRIME試験 (#3566)
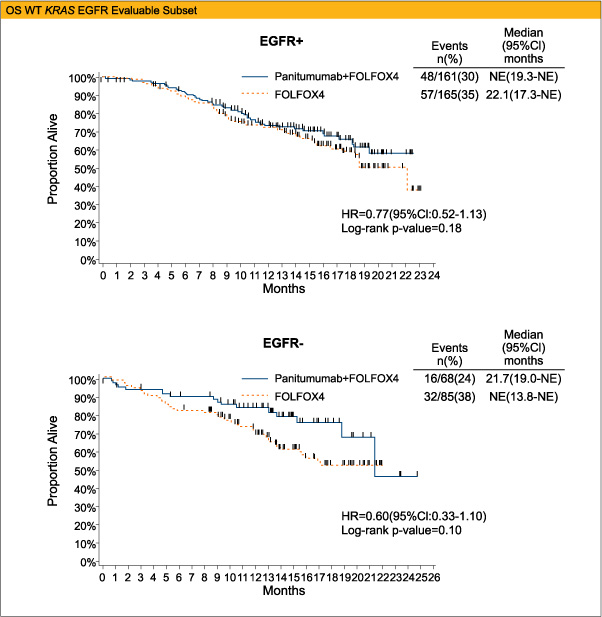
KRAS野生型でかつEGFRの評価が可能であった症例は、FOLFOX4+Pmab療法群で229例[EGFR (+) 161例、EGFR (-) 68例]、FOLFOX4療法群で250例[EGFR (+) 165例、EGFR (-) 85例]であった。
PFS中央値は、EGFR (+) ではFOLFOX4+Pmab療法群で10.4ヵ月、FOLFOX4療法群で8.0ヵ月 (HR=0.75、95%CI:0.56-1.00、p=0.05)、EGFR (-) では各々11.3ヵ月、9.3ヵ月 (HR=0.78、95%CI:0.52-1.18、p=0.24) であった。
また、OS中央値はEGFR (+) ではFOLFOX4+Pmab療法群で未到達、FOLFOX4療法群で22.2ヵ月 (HR=0.77、95% CI:0.52-1.13、p=0.18) 、EGFR (-) で21.7ヵ月、未到達 (HR=0.60、95%CI:0.33-1.10、p=0.10) 、ORRはEGFR (+) で54%、52%、EGFR (-) で63%、51%であった。
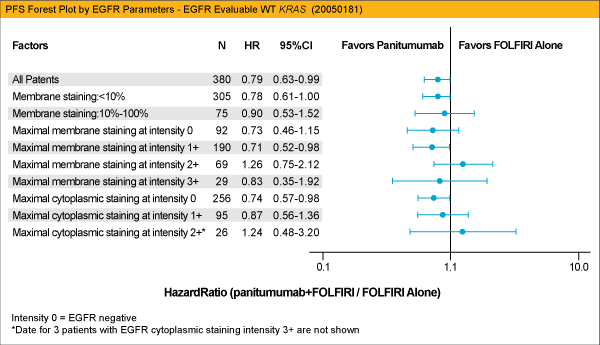
なお、両試験において、EGFRの染色強度による解析が実施されたが、染色強度とPFSおよびOSとの関連は認められなかった (下図は20050181試験)。
免疫組織化学染色におけるEGFR発現の有無はPmabの効果予測因子とはならなかった。また、FOLFIRI療法およびFOLFOX4療法を施行された症例の予後予測因子ともならなかった。
20050181試験は切除不能進行・再発大腸癌の二次治療においてFOLFIRIに対するPmabの上乗せ効果を、PRIME試験は切除不能進行・再発大腸癌の一次治療においてFOLFOX4に対するPmabの上乗せ効果を検証した多国間共同の第III相臨床試験である。両試験ともにKRAS野生型の症例においてPmab併用群で有意にPFSが勝っており、一次治療でも、二次治療でもPmabの有用性が証明された試験である。
今回、本来の標的分子であるEGFRの発現を免疫組織化学染色で評価し、Pmabの効果予測因子 (predictive marker)、Pmab非併用群の予後予測因子 (prognostic marker) の可能性について検討した。その結果、免疫組織化学染色によるEGFRの発現は効果予測因子にも予後予測因子にもならなかった。やはり抗EGFR抗体の治療効果予測には、KRASが最も重要な因子であることが改めて確認された。幸い我が国では、Pmabの使用に際してEGFR発現の測定は求められていない。
(レポート:山崎 健太郎 監修・コメント:寺島 雅典)