ケースカンファレンス~トップオンコロジストはこう考える~
監修中島 貴子 先生聖マリアンナ医科大学
臨床腫瘍学
日常診療で遭遇する症例を取りあげ、トップオンコロジストが治療方針を議論するケースカンファレンスをお届けします。
CASE6
2017年10月開催
PS不良の大腸癌多発肝転移例
に対する治療戦略
 牧山 明資 先生
牧山 明資 先生
JCHO 九州病院
血液・腫瘍内科 加藤 健 先生
加藤 健 先生
国立がん研究センター
中央病院 消化管内科
 小髙 雅人 先生
小髙 雅人 先生
医療法人薫風会 佐野病院
消化器がんセンター 坂井 大介 先生
坂井 大介 先生
大阪大学大学院
医学系研究科 先進癌薬物療法開発学寄附講座
- 症例プロファイル①
- ディスカッション 1
PS不良の盲腸癌
多発肝転移に対する治療 - ディスカッション 2
盲腸癌切除後の多発肝転移
増悪に対する治療 - 症例プロファイル②
- ディスカッション 3
黄疸を伴うPS不良の大腸癌多発肝転移の治療方針 - まとめ
ディスカッション 3 黄疸を伴うPS不良の大腸癌多発肝転移の治療方針
S状結腸癌多発肝転移で黄疸がある場合の治療をどのように進めるか?
牧山もう1例提示します。症例は49歳の男性で、心窩部痛、腹部膨満感、下痢などで受診され、S状結腸癌の多発肝転移と診断されました。原発巣は狭窄していましたが、便は下痢便として出ていました。この方は、黄疸が強くて、総ビリルビン値は初診時から2.7 mg/dLまで上昇していましたが、トランスアミナーゼは正常範囲内、ALPとLDHは高値で、貧血は軽度でした。PSは2で、(画像では確認できませんが)腹水が下腹部から少し上まで貯留しているなど、原発巣の壁肥厚所見が認められます(図5)。
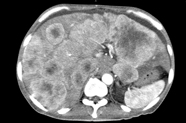 (図5)CT所見
(図5)CT所見
- 肝両葉に多数の腫瘤を認める。中等度腹水あり。
- S状結腸の壁肥厚所見あり
牧山かなり多数の肝転移があるRAS野生型の症例ですが、先生方の治療方針をお聞かせください。
坂井RAS野生型でcytoreductionを目指すのであれば、抗EGFR抗体薬は使用したいですね。化学療法については、肝機能への影響の少なさを考慮して、Oxaliplatinを選択してFOLFOXを行うと思います。減量も検討することになるでしょう。
牧山ほかの先生方は、この症例に対して2剤併用療法を選択されますか。
小髙総ビリルビン値が2.7 mg/dL、全身状態がPS 2で、RAS野生型の左側病変であれば、抗EGFR抗体単剤もあり得ると思いました。実際に、同様の病態の症例で、抗EGFR抗体単剤でかなり腫瘍が縮小し、その後、2剤併用療法+Cetuximabに切り替えた方も経験しています。
牧山加藤先生はいかがでしょうか。
加藤49歳で体力があるならば、総ビリルビン値が2.7 mg/dLでも、5-FUを減量する必要はないでしょうし、Oxaliplatinを減量する理由もありませんが、PS 2であれば、Oxaliplatinの相対用量強度を80%くらいで開始するのがよいと思います。ワンチャンスであることを考えると、RAS野生型であれば抗EGFR抗体を併用すると思いますので、FOLFOX+Panitumumabを選択します。全身状態は診察時に患者さんの顔をみて決めることも多いですね。
牧山ワンチャンスということを考えると、使用できる薬剤はなるべく使用して、しっかり治療したいと考えますが、PS不良を考慮する抗EGFR抗体単剤も選択肢になるということですね。
FOLFOXのdoseに関しては臓器機能に応じて減量する、ただしOxaliplatinに関しては今回、それほど減量する必要はないというご意見でよろしいでしょうか。
坂井はい。Oxaliplatinは腎代謝、腎排泄ですから、その方向性でよいと思います。
牧山5-FUの減量を考える総ビリルビン値の目安はありますか。
加藤10 mg/dLでもフルドーズを使用できると記載のある教科書もありますが、さすがに5 mg/dLを超えたら半量への減量を検討します。
坂井私も3~5 mg/dLが一つのラインにはなると思います。
小髙私は5 mg/dLで判断するようにしています。
牧山先生方のご意見をまとめると、総ビリルビン値が5 mg/dLを超えてくると、減量もしくは使用自体を控えるということになりますね。
その後の治療経過
牧山この患者さんにはFOLFOXを80% doseで投与し、抗EGFR抗体も併用しました。その結果、1ヵ月後には肝転移が著明に縮小、その後も治療継続に伴って腫瘍は縮小しました(図6)。この方は神経障害が出て、途中でOxaliplatinを中止しましたが、約2年間、病勢をコントロールでき、皮膚障害を管理しながら仕事にも復帰しました。
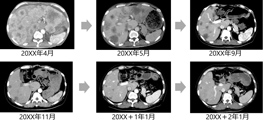 (図6)治療経過
(図6)治療経過
20XX年4月mFOLFOX6(80% dose)+抗EGFR抗体開始、T.Bil正常化。3コース目よりfull doseへup。20XX年12月よりL-OHP off(神経障害)。20XX+2年1月まで無増悪確認。皮膚障害のマネジメントを行いながら仕事を継続。
牧山黄疸例に対しても設樂先生が検討されており、総ビリルビン値2.0 mg/dL以上の肝転移7例にCetuximab単剤を投与したところ、1例では腫瘍が縮小し、他の6例でも黄疸が改善したと報告しています3)。6例がKRAS野生型で、1例は治療を急ぐ必要があったため、変異の有無が分かる前にCetuximabを投与したそうです。こちらもsidenessに関しては、情報はありません。cytoreductionを要する症例では、なんとか2剤併用療法、もしくは抗EGFR抗体薬を使用しようと試みているのは納得できます。
PS不良や黄疸のある症例に対する化学療法について、先生方のお考えをお聞きしました。2症例目はワンチャンスということで使用できる治療薬はしっかりと使用することが重要ですが、その一方で、全身状態が不良であることを考えると、抗EGFR抗体単剤投与や化学療法の減量も考慮し、安全性に重きを置いた考え方もあると思います。
最後に、全身状態不良例でcytoreductionを考える際、sidenessをどのように考えるか先生方のご意見をお聞かせください。

小髙今はsidenessを考慮するのが基本です。左側病変例には抗EGFR抗体を検討しますし、右側病変例であればFOLFOXIRIが施行できる方にはFOLFOXIRI+Bevacizumabを第一選択とし、できない方には右側であっても抗EGFR抗体の使用を考慮します。
牧山腫瘍縮小を目指す場合には右側であっても抗EGFR抗体の使用を考慮されるのですね。
小髙ただし、効果判定は短期間で行い、おそらく1ヵ月後にはCT検査を行い、腫瘍が縮小していなければ切り替えます。
牧山坂井先生、いかがでしょうか。
坂井基本方針は小髙先生と共通しています。右側病変には、抗EGFR抗体よりもFOLFOXIRIに重きが置かれるかと思います。左側病変には、抗EGFR抗体を優先でもよいと思います。右側病変例でFOLFOXIRIが難しい場合には、やはり抗EGFR抗体を選択し、早めに抗腫瘍効果を評価して継続・変更を検討すると思います。
牧山加藤先生はいかがでしょうか。
加藤ほぼ同意見で、右側病変ではCetuximabの有効性はそれほど期待できませんから、cytoreductionを目指すのであればFOLFOXIRIを選択します。右側と左側では治療の考え方は異なると思います。
牧山FOLFOXIRIが使用できない場合はどうされますか。
加藤その場合はFOLFOX、RAS野生型であればFOLFOX+Panitumumabを選択します。
坂井加藤先生、その場合、Bevacizumabの併用は選択肢にならないのでしょうか。
加藤Cytoreductionを期待するのであれば、Bevacizumabの優先度は低くなると思います。Disease controlを目指すのであれば、Bevacizumabも選択肢になります。
牧山先生方との討論を通じて、PS不良の肝転移例に対する治療方針の考え方が明確になったと思います。貴重なご意見、活発なご発言、ありがとうございました。
GI cancer-net
消化器癌治療の広場
